�z�����䪚�صĺ˚��Y�����ɞ�һ�N��ǰ����ˎ���f��ϵ�y�������b�d؛����M�й�������S�����߯����İlչ����ԭ��ˎ����ߴ̼����ӻ����ѱ��������z���У��Ԍ��F��ؓ�dЧ�ʺͿɿ�ጷţ��Ķ�����ί�Ч�����[�����P���ɼ��������[���h���е��P�I������������͘O��ֱ��Ӱ푿��[������Ч������ǰ�����z���d�w���ί����Զ���ه��Դ�����{����������ɼ���������x���f��ϵ�y���������{�����ܣ��ɞ������[�������ί�Ч�ʵ���Ҫ����
�о��l�F���ǻ�������ͨ�^�������P��̖ͨ·������D�������B��NF-��B���ͽz��ԭ�����ø��MAPKͨ·���T�����ɼ���M1�O��������һ�N�ϳ��ǻ������ķ����������·�����һ�N��ø�ٷ������漰�����|�����ɰ����c߀ԭ�ǵ��ʻ�֮�g�ķ������@��һ�N��Ȼ�l�����^�̣�����Ҫ�~��Ļ��W���|�����ҿ����ڰ�ȫ�Ϳɿصėl�����M�С�D-��¶�ǣ����º��Q����¶��������һ�N߀ԭ�ǣ��ڱ�������ͨ�^C�����������w�R�e�͔zȡ���������{��������Ҫ���á���ˣ���¶���ǻ����ĵ����|���܌����ɼ������F�����H�����������{��Ч�������w���ԣ��F���о������ǻ������e��ه�����ǻ����ܸ�׃�����|�����M���T�����ɼ������_���������ӣ���TNF-����IL-1�����F�֮ǰ���о�չʾ��ͨ�^��ţѪ��������ݣ�BSA MBs���ϽM�b����-��ӾW�j��һ�����ɹ������z�ҡ���ˣ������Mһ�����O��¶���ǻ�����BSA��Man-BSA�����H���������z���Ƃ��ģ�壬����߀�����������z�����T�����ɼ����O�����Ķ��x���z�ҹ��е������{�����ԡ�


�D1. ��¶�ǻ��Ľ���-����z�ҵ��Ƃ估��錧M1�;��ɼ����O�����{���[�����������ęC�� ���DԴAdvanced Science��
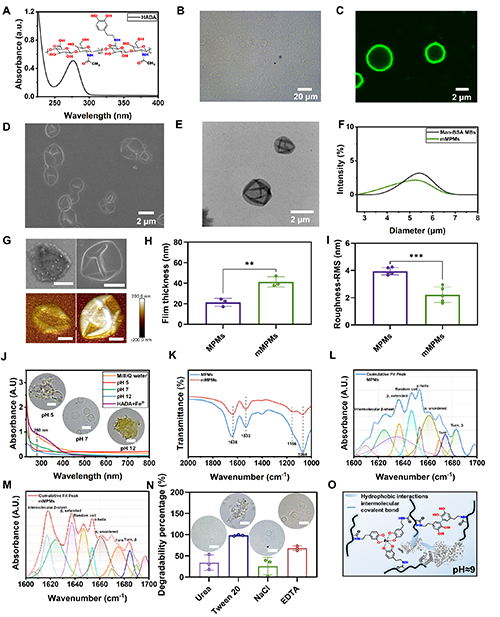
�D2. HADA�ĺϳ��Լ�mMPMs���Ƃ䣨�DԴAdvanced Science��
ԭ��朽ӣ�https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202415565
- ��ۿƼ���W��ڽ��ڈF� Adv. Mater.���C���W���o����������ۺ��z�һ��Ķ��������OӋ��ʽ 2026-01-25
- �������Ʊ���/�������/�V��ꐘ��� AM��ͨ�^�z�������|�lԭλ�ۺό��F���L�Ҝ��� - ���ڸߌ��ȶȓp����ҕ�������� 2025-11-24
- �A�ώ����� Small���w�S�ؼ{������Ƥ������Һ���Ƃ�ߝ��ᡢ����׃ɫ����׃�����z�Ҽ���������Ϳ���ϵđ��� 2025-07-09
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- �칤����x/���ƽ��F� ACS Nano�����¼{��ø���������[�����Ⱦ� �����Yֱ�c�������ί�ͻ�� 2026-02-20
