�[�������ܰͽY(tumor-draining lymph node, tdLN)���[�������D�Ƶ��T����Ҳ���m�������ߑ���l����ʼ�l��λ���mȻ�����ܰͽY�и����д�����ͻ�����DCs�����ܰͼ����������m�^�����[��������̼����{���� T ������TRegs���e�ۣ����l�������ܣ�������DCs���켰Ч��T������U�����o���a����Ч�Ŀ��[�����ã������[���������ݲ��D�ơ���ˣ����D�[�������ܰͽY�ľֲ��������ƣ������[����ԭ�خ��Ե�Ч�� T ������U�������ܿ��[�������h�����Ǹ����[�������ί�Ч��ؽ����Q�ĿƌW���}��
ᘌ��@һ���}���Ї������W�������ڈF����ü{�ͺ�������OӋ�������|�ᣨHA������ᘞ���|��ؓ�d�{�ׂ��f�w�����f�w�����b����͆�Ӳ֬�ᣨGMS��������|�ᣨT-HA-GMS���������B�� CD40�����w����CD40�����Ȳ����d������PolyI:C�����P��ԭ���Y�Ϧ�PD1�ͺϽoˎ�������[�������ܰͽY�������硣�ͺ������܉��l�{������ݔ�ͺ��خ������ߑ������D�[�������ܰͽY�������ƣ��������[��Ч����
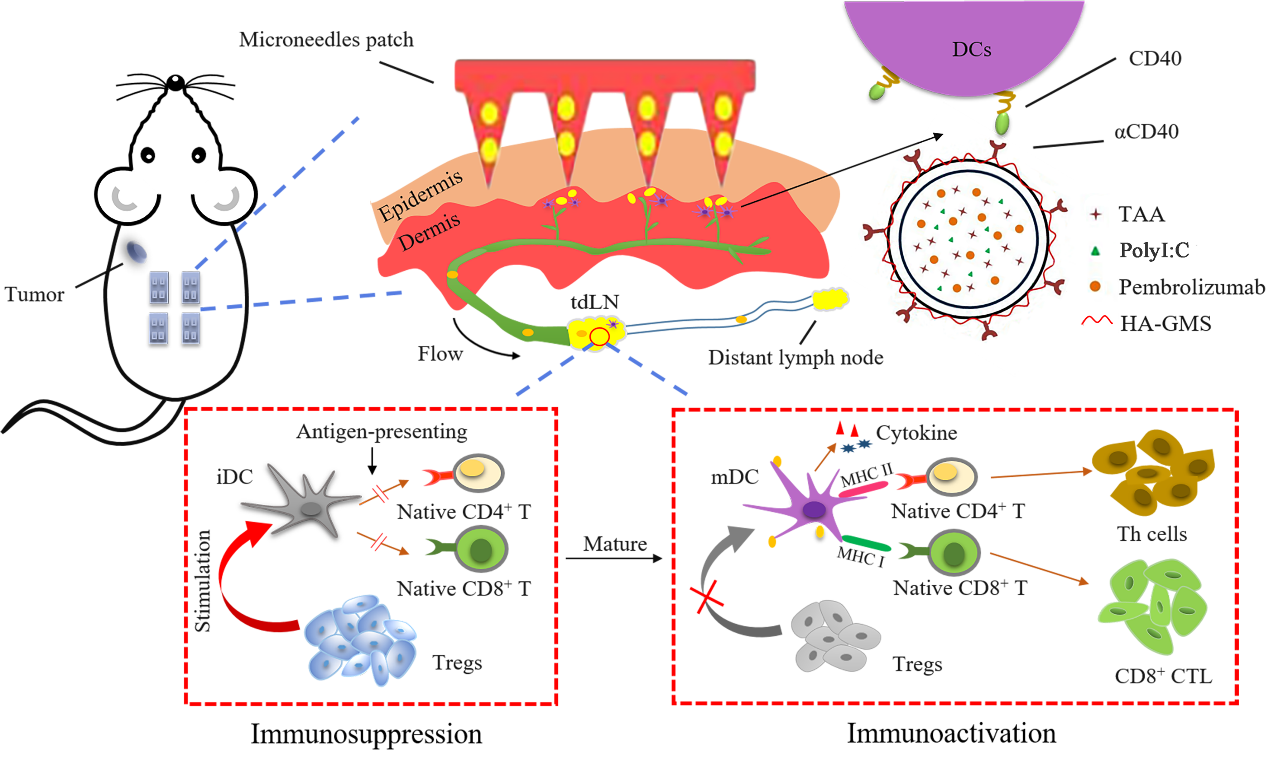
�D1. ���ܻ����f�wͨ�^ᘽ�Ƥ�oˎ����tdLNs���T�����ߑ���ʾ��D
ԓ�F����ú�ɫ������B16F10������С��ģ��ͨ�^����۽������@�R�����^��ͼ�����ʽӋ�������yӋ�������ͺς��f�w�����@���DCs�����zȡ�������M�������ӵı��_���p��TRegs��tdLNs���۷e��������Ч��T�ܰͼ������[��������

�D2. �ͺς��f�w�������зֲ��Լ��خ��Կ��w���������ӱ��_
�F�ͨ�^�����CD40�����OӋ���F�ˏͺς��f�w�ܰͰ������ã����ұ�����ˎ�������K�����K��Ƣ�K�Լ��I�K�е����^Ч�������MIFN-���� IL-2 �ı��_������Ҫ���Ǐͺς��f�w�����@�ļ���Th1�ͼ�������ƫ��
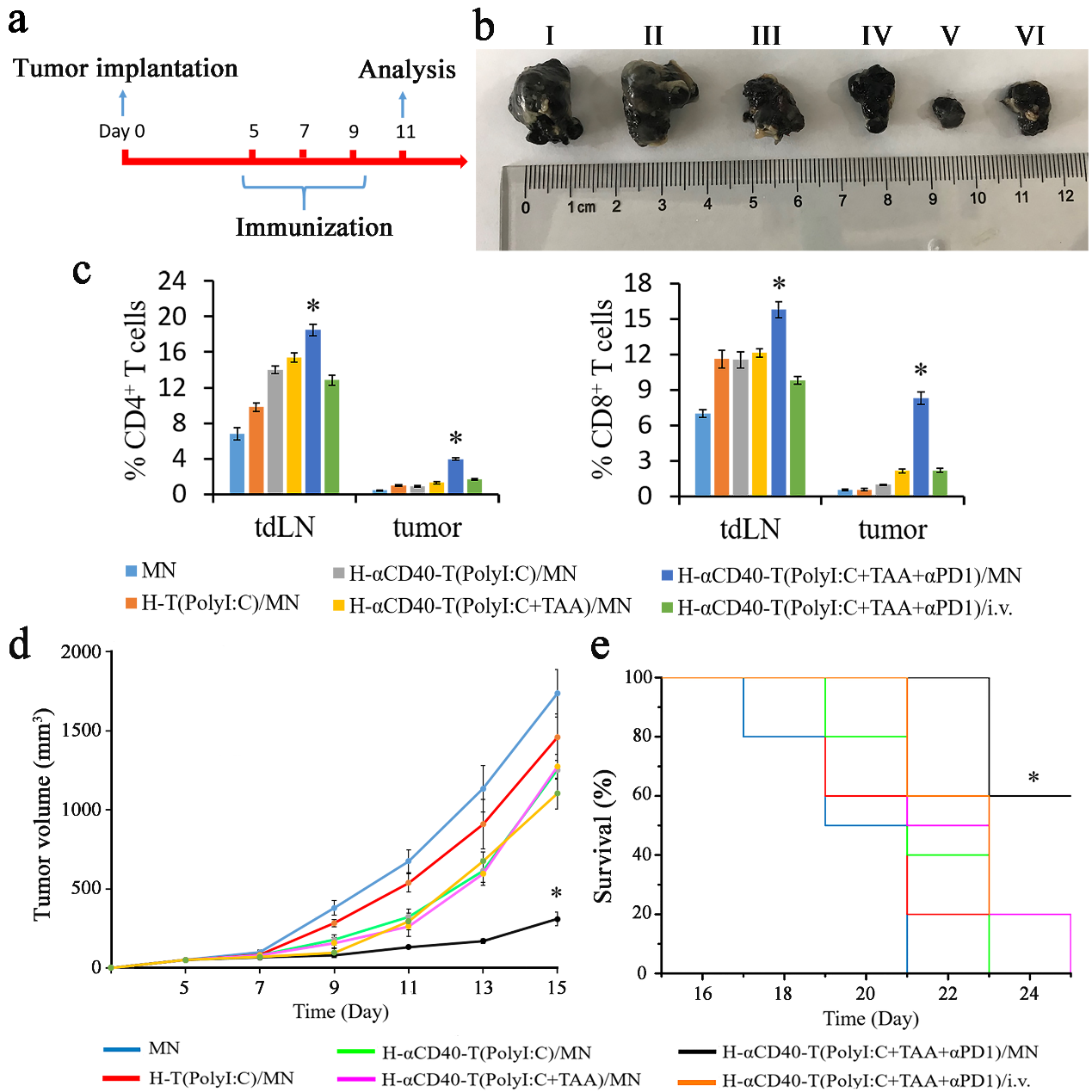
�D3. �{�ͺ�������Ϧ�PD1�ί����L����С������r�g��
ԓ�Fꠌ��F�˂��f�w�ܰͽY����ݔ�͡���ͻ����R�e�zȡ�����졢���ȶ�λ����ԭ������f��Ч�� T ������U���������[�������D�[�������ܰͽY�������ơ����[�����ߵ��о����R�����÷����ṩ����˼·��
���о���Reverse immune suppressive microenvironment in tumor draining lymph nodes to enhance anti-PD1 immunotherapy via nanovaccine complexed microneedle���}�l����Nano research���Ї������W��ԓՓ�ĵ�һ��λ����ʿ�������������µ�һ���ߣ�����������Փ��ͨӍ���ߣ�Փ�Ĺ�ͬ���ߞ��Ї������W������������о��Fꠎ��^������V���������Ŀ�õ��ˇ�����Ȼ�ƌW������Y����
Փ��朽ӣ�https://link.springer.com/article/10.1007/s12274-020-2737-5
- �칤����x/���ƽ��F� ACS Nano�����¼{��ø���������[�����Ⱦ� �����Yֱ�c�������ί�ͻ�� 2026-02-20
- ɽ�|��W�������ڈFꠡ�Adv. Mater.������������������ˮ���z���� - ���F���Ի��[�������ί���ͻ�� 2025-10-09
- �㽭��W����Fꠡ�Cell���ӿ�����ˎʳͬԴ����-�S�ζ���ϵ�y�p�������ί������¼���������Ч 2025-08-26
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
