�z�|(zh��)�������И���(j��ng)ϵ�y(t��ng)�O�����u�Ե��[����������u�ԡ��z�����|(zh��)�Ժ�Ѫ�X���ϣ�BBB�����o(h��)�����y(t��ng)����Ч��Ƿ�ѡ�����������SDT������o��(chu��ng)����ӽM�����ȃ�(y��u)�ݳɞ����d�ί���ʽ��ͨ�^�������a(ch��n)���ξ��B(t��i)���Ɖ��[����(x��)����ͬ�r�����ջ�Ч��(y��ng)����(qi��ng)ˎ��B����С���������w��(n��i)���x�졢�x���Բ�Ȇ��}�������˯�Ч���M�ܼ{���d�wϵ�y(t��ng)�������������M(j��n)�����ܴ��^BBB���F(xi��n)�z�|(zh��)���f(xi��)ͬ�ί����d�w�O(sh��)Ӌ�Ծ�����(zh��n)��
���Ե��טӶ��ģ�ELPs������ģ�M��Ȼ���Ե����˹����ģ��{�����������Ժá�����ԭ�Ե͡���푑�(y��ng)�Լ��ɱ�����ø����ȃ�(y��u)�ݣ��������t(y��)�W(xu��)�I(l��ng)������P(gu��n)ע��ELPs��VPGXG���Ć�Ԫ��(g��u)�ɣ���ͨ�^���ж��ƌ��F(xi��n)���ضȡ�pH��ȴ̼���푑�(y��ng)�����ԽM�b�О�ʹ����ؓ(f��)�d��ˮˎ����Lˎ��ѪҺѭ�h(hu��n)�r�g�����ˎ���������öȡ�������c�����x����λ�γɵĽ��ٷӾW(w��ng)�j(lu��)��MPNs�����[�����W(xu��)�����W(xu��)�ί���CDT���ʹŹ���MR��������չ�F(xi��n)�������e�džΌ���/Mn2?��TM��MPNs���������������ԡ�pH�����Ժ�CDT���ܡ����S���ķ��u��ʹ�������Ϳ�Ӳ��������ڼ{�ײ����ϡ����⣬�о�������������ROS����ֱ�Ӛ����[����(x��)���⣬߀��ͨ�^�T��(d��o)����ԭ�Լ�(x��)��������ICD���ͼ���cGAS-STINGͨ·�|�l(f��)���[�����ߡ�Mn2?������(qi��ng)cGAS��DNA�������Լ�cGAMP�cSTING���H�������f(xi��)ͬCDT/SDT��Ч����[�����߷���(y��ng)��
���ڴˣ��|�A��W(xu��)ʷ��ꖽ��ڈF(tu��n)��c�����������W(xu��)S��bastien Lecommandoux�����n�}�M�����O(sh��)Ӌ����(g��u)����һ�N���ɼ�(x��)��Ĥ�����Ľ���-��ӾW(w��ng)�j(lu��)�������Ե��טӶ����z�����ڌ��F(xi��n)ԭλ�X�z�|(zh��)��������/���W(xu��)����/�����ί����D1�����о��F(tu��n)��Է�������33.7kDa�����������О�MW[VPGVG-VPGMG-��VPGVG��2]20��ELPͨ�^���r�I�c����߲��e6��Ce6��朽�������ˮ��Һ��ͨ�^�ԽM�b�γɼ{���z�����S������ɆΌ����Mn2+�M�ɵ�MPN���Ķ��@��Ce6-ELP@TM�����Ce6-ELP@TM�����ɼ�(x��)��Ĥ��MMs�����b�@�ü{��ˎ��Ce6-ELP@TM/MM��ԓ�{��ˎ����������W(xu��)���ԡ��w�⼰�w��(n��i)�Ŀ��[��Ч����������Ч�������P(gu��n)�C(j��)�Ʊ�Ԕ��(x��)�u�r��

�D1. Ce6-ELP������ĺϳɣ�a����Ce6-ELP@TM/MM���Ƃ������ԭλ�X�z�|(zh��)���ί�ʾ��D��b����
�F(tu��n)�����ͨ�^1H NMR���ɹ���V���ӑB(t��i)��ɢ�䡢�A��ɫ�V��TEM���C����Ce6-ELP@TM/MM�ijɹ��Ƃ����Ҿ������õ��z�w��(w��n)���Լ������W(xu��)��������ƽ���ߴ�s��58 nm���D2����

�D2.��a��Ce6-ELP��뮻�DMSO�е�1H NMR�V����b��ELP��Ce6-ELP�ğɹ�l(f��)����V�����l(f��)���L = 405 nm������c����������ɹ�̽ᘜy���õ���Ce6-ELP�{���z����CMC����d����ͬ̎����Ce6-ELP�{���z����ˮ�����ߴ�ֲ�����e����ݗ��ǰ��ELP��Ce6-ELP�ĈA��ɫ�V����f-g��Ce6-ELP@TM����D��Ce6-ELP@TM�ijߴ�ֲ�ֱ���D����Ce6-ELP@TM/MM��TEM�D��������50 nm������h��Ce6-ELP@TM/MM��ɢ��ˮ�С�PBS����10% FBS��DMEM�е�ˮ�����W(xu��)�ߴ磨n = 3������i���ڳ�ݗ�պ��TEMP���@��1O2��ESR�V�D��[Ce6] = 5 ��g/mL, 1.0 MHz, 1.0 W/cm2, 30 s����
�S�F(tu��n)�ͨ�^��ʽ��(x��)���g(sh��)�ͼ���۽��������[����(x��)����Ce6-ELP@TM/MM�Ĕzȡ�О飬����CCK-8�������u���˼{��ˎ����w�⿹�[��Ч�����D3�������Դ˽Y(ji��)���_���˺��m(x��)����г�ʩ�ӵėl����ˎ��ʹ�Ý����
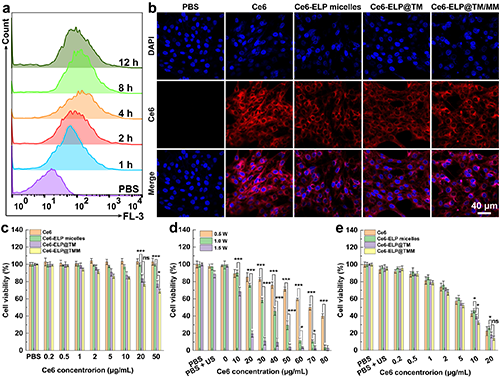
�D3. ��a��C6��(x��)���cCe6-ELP@TM/MM���B(y��ng)��ͬ�r�g�����ʽ��(x��)���g(sh��)�z�y�Y(ji��)����n = 3����C6��(x��)���c��ͬ���Ϸ���4С�r��ļ���۽��D��b����������40 ��m������c���ڛ]�г�����r�£�C6��(x��)���c��ͬ�������B(y��ng)24С�r���������n = 6������d���ڲ�ͬ�l���£�Ce6�cC6��(x��)�������B(y��ng)��(j��ng)��ͬ�l�������䣨1 MHz����������n = 6������e����ͬ�����cC6��(x��)�������B(y��ng)���ڳ������µļ�(x��)��������1 MHz��1 W/cm2��40 s��n = 6�����ڈDc-e�У�ns��ʾ�o�y(t��ng)Ӌ�W(xu��)���*��ʾp < 0.05��***��ʾp < 0.001��
�������F(tu��n)������о���Ce6-ELP@TM/MM��C6��(x��)����Ԕ��(x��)�ί��C(j��)�ơ�ͨ�^��(x��)������Ⱦɫ����(x��)�������Լ���(x��)����(n��i)��ROS�������wĤ�λ�ȵęz�y�C���ˣ�ԓ�{��ˎ��Ļ��W(xu��)�����W(xu��)�������W(xu��)�ί�Ч�����D4�����������|(zh��)����ӡ�E�����u��������(x��)����(j��ng)�{��ˎ��̎����(x��)����(n��i)��STINGͨ·�ļ����B(t��i)���C����Mn2+�ڼ�(x��)��STINGͨ·�����^���е����á�

�D4.��a����ͬ����̎��C6��(x��)���ڳ����ڻ��ڗl���µĻ��Ⱦɫ�Y(ji��)����������= 100 ��m������b����(j��ng)��ͬ̎�����C6��(x��)���ĵ�����ʽ��(x��)���g(sh��)������n = 3������c-f����(j��ng)��ͬ̎����C6��(x��)����(n��i)ROSˮƽ׃������ʽ��(x��)���z�y�Y(ji��)��������������n = 3������g����(j��ng)��ͬ̎�����C6��(x��)����(n��i)�ľ����wĤ�λ׃���z�y�Y(ji��)����������= 20 ��m��1 W/cm2, 30 s, 1 MHz�����ڈDd��f�У�**��ʾp < 0.01��***��ʾp < 0.001��
�F(tu��n)��M(j��n)һ���о��˼{��ˎ���ڳ�ݗ�����T��(d��o)����Դ�Լ�(x��)��������Ч����ͨ�^����ATP��HMGB-1�о�������۽��@�R�^����������ݗ���£��{��ˎ���܉�?q��)��?/span>ATP���ڼ�HMGB-1ጷ����ӣ��D5b-c����ͬ�r���������(n��i)������CRT�ⷭ����(x��)��Ĥ�ϣ��D5d�����Ķ��f��������w���T��(d��o)����(x��)���l(f��)������ԭ���������S��Transwell����C���������ICD�܉�������ͻ��(x��)���컯���D5e����

�D5.��a����(j��ng)��ͬ����̎����C6��(x��)����(n��i)��-H2AX�����ߟɹ�Ⱦɫ�Y(ji��)������ͬ̎����C6��(x��)��ጷ�ATP��b����HMGB1��ˮƽ��c����C6��(x��)��Ĥ���汩¶CRT��ˮƽ��d������ͬ̎����C6��(x��)���c��ͻ��(x��)��������ʾ��D����ͻ��(x��)���컯��r��e�����ڈDc-d�У�**��ʾp < 0.01��***��ʾp < 0.001��
ԓ�{��ˎ��y����Mn2+��Ce6�քe�߂�MR����͟ɹ��������ԣ�ͨ�^�����ɼ�(x��)��Ĥ����ǰ��ļ{��ˎ�����X���ۼ���r�ķ�������C��Ce6-ELP@TM/MM�܉��ԽѪ�X���ό��F(xi��n)��Ч���X���f�ͣ��D6����

�D6.��a��β�o�}ע��Ce6-ELP@TM��Ce6-ELP@TM/MMǰ��ͬ�r�g�c���ԭλ�X�z�|(zh��)��С��ģ�͵�T1�ә�(qu��n)MR�D��b��β�o�}ע�䲻ͬ�r�g�c��ԭλ�X�z�|(zh��)��С��ģ�͵��w��(n��i)�ͣ�c���x�w�����ɹ�D��ͬ̎���M����С����z�|(zh��)��MR��̖��(qi��ng)������������d�����ɹ⏊(qi��ng)�ȷ�����e�����x�w��Ҫ���ٟɹ⏊(qi��ng)�ȷ�����f����[Ce6] = 5 mg/kg��ÿֻС��200 mL PBS��n = 3�����ڈDd-f�У�ns��ʾ�o�y(t��ng)Ӌ�W(xu��)���*��ʾp < 0.05��***��ʾp < 0.001��
�S�F(tu��n)�ͨ�^����C6ԭλ�X�z�|(zh��)��ģ�ͣ��о���Ce6-ELP@TM/MM���w��(n��i)���[���ί�Ч�������Y(ji��)����������ͬ����̎����ʩ�ӳ����@����(qi��ng)���ί�Ч��������������[�������L���@���������ί�(li��n)�ϻ��W(xu��)�����W(xu��)�ί���Ȇ�һ�Ļ��W(xu��)�����W(xu��)�ί�Ч�����ѣ��D7����ͨ�^���߽M�������ߟɹ���Ƭ�M(j��n)һ����C�˼{��ˎ����w��(n��i)�ί�Ч���������w��(n��i)��STING�ļ�����r��

�D7.��a��Ce6-ELP@TM/MM�{��(f��)����ĺ���С���w��(n��i)�ί��^��ʾ��D����b����ͬ�ί��M�Ĵ�����MR�D��1��PBS��2��PBS + US��3��Ce6-ELP@TM��4��Ce6-ELP@TM + US��5��Ce6-ELP@TM/MM����6��Ce6-ELP@TM + US���Լ���ͬ̎������M�����[���w�e��c����С���w�أ�d������������c-d�M��n = 5������e���[�������߽M�����W(xu��)��H&E��TUNEL�������ߟɹ�Ⱦɫ��p-STING���Y(ji��)������(bi��o)�ߞ�50 ��m�����ڈDc�У�*��ʾp < 0.05��**��ʾp < 0.01��***��ʾp < 0.001��
�S�F(tu��n)��о���Ce6-ELP@TM/MM�{��ˎ��錧(d��o)��(li��n)���ί�����w��(n��i)����푑�(y��ng)���Y(ji��)��������Ce6-ELP@TM/MM��ʩ�ӳ����[����Ƣ�KCD4+T��(x��)����CD8+T��(x��)���Ĕ�(sh��)�����{(di��o)������@���[����λ���{(di��o)��(ji��)��T��(x��)����Tregs���@�����{(di��o)���C��ͨ�^����/���W(xu��)����/����(li��n)���ί����܉���Ч�̼��C(j��)�w�a(ch��n)������Ě�����Ч��(y��ng)��T��(x��)�����Ķ�����(qi��ng)���[���ί�Ч�����D8����

�D8. ��ͬ̎����Ѫ����TNF-����a����IFN-����b����IL-6��c��������ˮƽ��n = 3������ͬ̎�����X��(n��i)CD11c+CD80+DC�İٷֱȣ�n = 3����d������e����ͬ̎�����X��(n��i)CD3+CD4+ T��(x��)���ͣ�f��CD3+CD8+ T��(x��)������ʽ��(x��)�������Y(ji��)����n = 3������g����ͬ̎����Ƣ�KCD3+CD4+ T��(x��)���ͣ�h��CD3+CD8+ T��(x��)������ʽ��(x��)�������Y(ji��)����n = 3����a-d�M�У�**��ʾp < 0.01��***��ʾp < 0.001����
�����о�����Biomimetic metal-phenolic network-coated elastin-like polypeptide micelles as an immunogenic cell death inducer for orthotopic glioma sonodynamic-chemodynamic-immune therapy�����}���l(f��)���ڇ��H�����ڿ�Nano Today�ϡ��|�A��W(xu��)�����c�t(y��)�W(xu��)���̌W(xu��)Ժ��ʿ�о�����־��(qi��ng)���һ���ߣ��|�A��W(xu��)ʷ��ꖽ�����ͨӍ���ߡ�ԓ�����õ��ˇ�����Ȼ�ƌW(xu��)����ί���Ϻ��п�ί���Ŀ���Y����
ԭ��朽ӣ�https://doi.org/10.1016/j.nantod.2025.102810
- ���_��W(xu��)ꐴ�ȫ���ڈF(tu��n)ꠣ��Y(ji��)�����t(y��)ˎ����(j��ng)��Փ����(g��u)�����ڽ۹����ǵľ��ɼ�(x��)��Ĥ�����{���d�w���ڰ�������Լ�ƽϢ��(x��)�������L(f��ng)�� 2022-02-11
- �|�A��W(xu��)ʷ��ꖽ����n�}�M��ACS Nano�������ɼ�(x��)��Ĥ�����Ķ�ܼ{�����z����MR��������(d��o)��ԭλ�X�z�|(zh��)��(li��n)���ί� 2021-12-06
- �Ĵ���W(xu��)�ߕ��������n�}�MBiomaterials�����ɼ�(x��)��Ĥ�����ļ���푑�(y��ng)�Լ{���fˎϵ�y(t��ng)�����[���������ί� 2020-06-23
- �A������߅�������w�i������������ڈF(tu��n)� Nat. Chem.���_�l(f��)����(qi��ng)ˮ�¡��f���z�� - �`��Դ�Ժ������� 2026-03-31
- ���t(y��)��һ��Ժʢ�������/�A�ƴ��R������ AFM����(g��u)���˷������ˮ���z�NƬ-�ڼ���p���ί�����ȡ�����M(j��n)չ 2026-03-02
- ����������·���ڈF(tu��n)� AFM���ġ����顱���ֵ��IС������{���w�SĤ - ���F(xi��n)�{��Һ��ͨ�����x 2026-02-25
- �|�ϴ�W(xu��)�����۽����n�}�M Small���������ϽM�b����-��ӾW(w��ng)�j(lu��)һ���Ƃ书���Գ����z�� 2023-08-30
�\���P(gu��n)ע�߷��ӿƼ�

- ���a(ch��n)���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)���h����...
- ��ˎ����Ч����������PMEC C...
- 2026����ߌ��Ї�����Ұl(f��)չ...
- �����I(l��ng)Ʊح300+���h��I(y��)�R��...
- �P���Ж|�����L���Ѓx�����{(l��n)...
- �f����Ŀ �ذ��_�֣�2025�C(j��)...
- ICIE���H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_չ�ڼ����ۄ�������朄�δ...
- 9������Ҋ���£�AI�(q��)��+���a(ch��n)...
- �P(gu��n)���e�k�ڶ�ʮ�����Ї����H...
- �۳Ǵ�Steven Wang���ڡ��^...
- �����ֿƴ��䏩/�ǫI(xi��n)�¡���...
- ���������ƾ��_(d��)���ڡ������i...
- �A�ƴ��T�ض����ڈF(tu��n)� Macro...
- �����������/���t(y��)������� ...
- ������ꐏ�(qi��ng)���ڈF(tu��n)� Matter...
- �������մ�/���� AFM���w�S...
- �A������߅�������w�i������...
- ���A��W(xu��)���r�F(tu��n)� AFM���U�f...
- ���������x�����ڈF(tu��n)� Nat. ...
- �A�����������塢�V�|������...