������ē���ж������ж�đ֬���Ƕ��Ƴ�Ҋ���Ͷ�l�������ί�ԭ�t�鿹��Ⱦ����������ȥ�����R�������g�ί����Դ������ж�-��ͻ���|ȱʧ���y���Լ�������Ĥ���ɼ��M���h���L�ڸ�ˮƽ�װY�����¼����Ͱl���M��Ӱ� ���Ć��}����ˣ����ͬ�r��Ч�������ؙC���²����������װY����Ч�ޏ��ж�-��ͻ���|ȱ�p��һ�ؽ���Q�Ҿ��������Ե��y�}��
���ڣ��V���мtʮ�֕��tԺ���h���ڈF��c�V�|ʡ�ƌWԺ�����c�t�W�����о������������о��T�n�}�M�����OӋ��һ��ӑB���W�jROS푑��Ϳ�ע��ˮ���z�������ޏ��ж�-��ͻ�װY��B�µĹ��|ȱ�p��ԓˮ���z�ĄӑB���W�j�Ա������֦�ĺ������c��Alg-PBA����֧�c���ӑB���Ό���߀ԭ���y�{������(TA@Ag NPs)�Ͷ�Ͱ�������|��(HA-DA)��ͬ�����M�b��������õĿ�ע���ԡ��M��ճ���ԡ������Լ�ROS푑���ˎ��ጷ����ܣ�ʹ�佛ע�����䲢ճ���ڲ�ͬ�Π�ĽM��ȱ�p��λ�����������Ɖģ����m���M���\�ӣ��߂����õĽM�����m���ԡ�����ԓˮ���z�ɼ��r��ļ���O�����ɼ��������T�����������߷������܉�p���ж���ͻȱ�p�^���w�S�����γɡ����⣬ˮ���z���Ѓ��������������ԡ������Ϳ��������ܣ�ͨ�^��Ч���睓�ؙC���²��������ͻ�����ˮƽ���{�����ɼ���M2�O������Ч�p�p�ж����B�h���е��װY������푑����{�ظ�Ⱦ���ܓp�M���Ȳ��������h�����Ķ��@�����M��Ⱦ���ж�-��ͻ�ǽM��ȱ�p��������ޏ͡��C��չ�F��ԓˮ���z����һ�N���M�Ĺ����������ϣ��������ж�-��ͻ�װY��ȱ�p���|��������Ч�����I��ă�Խ����

ԓ��������ROS-responsive Adaptive Injectable Hydrogel Promoting Inflammatory Mastoid Bone Repair through Efficient Sterilization and Regulating Oxidative Stress and Macrophage Phenotype�����}�l���ڡ�Materials Today Bio���ϡ�ԓ�����õ��ˏV�����R�����¼��g�Ŀ���V���ЌWУ���ߵȣ�����I���Y���Ŀ���V�|ʡ�ƌWԺ�lչ����Y���Ŀ���V�|ʡ��Ȼ�ƌW�����Ŀ����֧�֣����ϴ�W�V�ݼtʮ�֕��tԺ�ˇ����ʿ���ַf�������t�������ϴ�W�V�ݼtʮ�֕��tԺ�c�V�|ʡ�ƌWԺ���t�������B��ʿ�о�����������Փ�ĵĹ�ͬ��һ���ߣ����ϴ�W�V�ݼtʮ�֕��tԺ���h�������V�|ʡ�ƌWԺ���t�����������о��T��Փ�ĵ���ͬͨӍ������
��ǰ�����������о��T�n�}�M��ͨ�^�M��ճ������ӻ��F��ROS푑��ӑB�I�ķ����OӋ���о��˶�N�{�ؽM���h�������M�M���������m��푑��Բ��ϡ���ACS Materials Lett. 2023, 5, 3142?3155��Chem Mater 2022, 34, 2655-2671��ACS Appl Mater Inter 2021, 13, 61638-61652��European Polymer Journal 2025, 225, 113723�������о������ǹ������n�}�M�c���h���ڈF��������h���{�ؿ�ע��ˮ���z���ж�-��ͻ����ȱ�p�ޏ��I������á�


�D1. ˮ���z���Ƃ䣺��a�� ��Ͱ���� HA �γɴ��ڃ���ӻ��F�� HA-DA;ͨ�^��֦�������c��ͨ�^ԭλ߀ԭ�Ό����Ƃ�{���y�w�����ϳ��˾��б�������F�� Alg-PBA;��b�� Ȼ�� TA@Ag NPs ���� HA-DA/Alg-PBA ˮ���z���|�У��Ԯa����K�� ROS ���ЄӑB�W�jˮ���z��
���ú��^𤸽ԇ�����r�iƤ�������ԇ������ӻ��F������ˮ���z�ĽM��𤸽���ܡ�ˮ���z����ָ�������Ƥ�w���������õ�ճ�����ԣ�ԓˮ���z�F���H��ճ������ָƤ�w���棬�����ܺܺõ��m����ָ���\�ӣ��oՓ��ָ��ֱ߀�Ǐ�����ˮ���z���ܱ���ԭ����ճ����B������������ē���ж������ж�đ֬����ɵ��ж������h���Е����^��Ļ����������ˮ���z�W�jROS푑��ԄӑB�������I�Ɍ��F�M���h���h��푑���ˎ��ጷš��ɈD2d-2g���о���֪��ˮ���z�ڻ������ĭh���Е�푑��Խ��⣬ጷ�TP@AgNPs��

�D2.ˮ���z�ĽM��ճ�����Ժ�ˮ���z�� ROS 푑��ԡ���a�� ˮ���z�F�Kճ�����ã����m����ָƤ�w���Π�;��b�� HA-DA/Alg-PBA/TA@Ag NPs ˮ���z��ˮ�Ќ��i��Ƥ�w��ͬ������F��������ճ����;��c�� ӛ�ˮ���z�е����z-���z�D׃;��d�� ˮ���z�� Ag+�۷eጷ�����;��e�� ���� Ag NPs ��ˮ���z�� PBS �� 0.3 mM H2O2 �еĽ���;��f����ͬ��r��ˮ���z�� ROS 푑���Û����;��g�� ʹ�ú��^���^��������@�R�f�������� ��ROS�� ���оW�jϵ�y���^�ΑB�ĈD������*p<0.05��** p<0.01��n=3����
�ɈD3���о���֪��ˮ���z���w��߂䃞�������������ԡ������Ϳ����������yԇ��ˮ���z��TP@Ag NPs��ʹ�䚢��97.85 %��S. aureus �� 99.10%��E. coli����D4a&b��ʾ��ˮ���z�����ɼ�����M2�O�����@�����M���á��Y���磨�D4c��e����ʾ����LPS�̼�����MSCs��HA-DA/Alg-PBA/TA@Ag NPs����Һ�з������@ʾ����e�����Ⱦɫ����ĵV���Y�����f��ˮ���z��MSCs�����ɹǵ������@�Ĵ��M���á�

�D3.ˮ���z�����������ԡ������Ϳ����������yԇ����a�� 48 С�r�Ļ�/���u����Ƭӛ�;��b�� 48 С�r��/���yԇ�ĽyӋ����;��c�� �� 1 �� 3 �� 7 ��� CCK-8 �����Y��;��d�� ˮ���z����Ѫ�О�;��e�� ����䁰�Ͷ����yӋ�Y��;��f�� ˮ���z�� DPPH ����Y��;��g�� TA@Ag NP �� DPPH ����Y��;��h�� ROS �ğɹⶨ���yӋ;��i�� �������y���D�� ��*p<0.05��** p<0.01��n=3����

�D4��ˮ���z�w��پ��ɼ����O����ٳɹǹ�Ч�� ��a���w����ɼ����O���ɹ��pȾɫ�ͣ�b��M1ָ��iNOS��M2ָ��PPAR�õĶ��������� ��c��d���ɹ����õİ붨�������� ��e����RAW264.7�������M��MSC�ijɹǻ��ԣ� ��*p��0.05��** p ��0.01��n = 3����
ˮ���z��TP@AgNPs��푑���ጷſ��{�����ɼ���M2�O�����Ԝp���װY������ͨ�^�����w���о���ԓˮ���z��ע��ɳ������ճ�����ж�-��ͻ��Ҏ�t��ȱ�p�Ă����Ȳ�����ͨ�^��Ч�Ŀ��������ס������������MѪ���γɺ����¹����������w���@���ӿ쌍�����ж�-��ͻ��Ⱦȱ�ڵ������M�̡���D5���D8��ʾ��
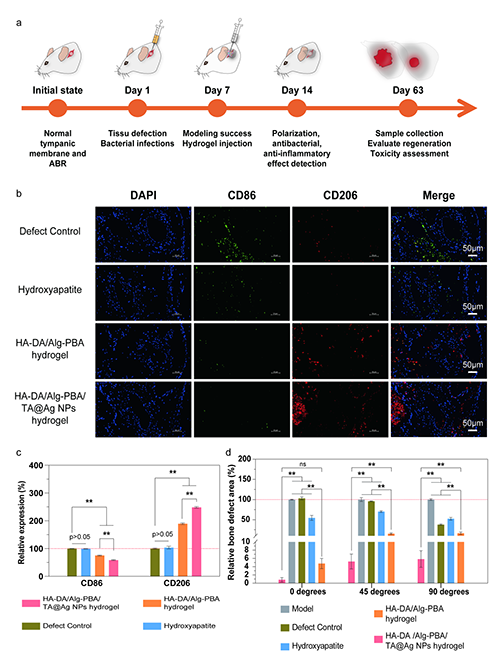
�D5��������w�Ⱦ��ɼ����O�������ĕr�g���� ��a������r�g���ĈD�� ��b���w�Ⱦ��ɼ����O���ɹ��pȾɫ�� ��c��M1��־��CD86��M2��־��CD206�Ķ��������� ��d���������Ķ�Ƕȶ����yӋ��*p ��0.05��** p ��0.01��n = 3����

�D6.�ж���ͻ�������� Micro-CT �u������a�� ���S����Ͷ�Ƕ����S�ؽ�;��b�� ���ܶȣ���c�� ���w�e/�M���w�e���Լ� ��d�� ��С����ȶ����yӋ ��*p<0.05��** p<0.01��n=3�������̶Ȟ� 1 mm��

�D7.�w�ȳɹǺ�Ѫ�����ɡ���a�� �w�ȳɹǵ����ߟɹ��u��;��b�� �ɹ�ָ�� OCN �Ķ����yӋ;��c�� ��Ѫ�ܼ���ָ�� CD31 �Ķ����yӋ;��d�� �w��Ѫ�����ɵ����ߟɹ��u�� ��*p<0.05��** p<0.01��n=5����

�D8.�� 63 ��� H&E �� Masson ��ɫȾɫ��������ɫ�����α�ʾ�ɹǼ����ͳɹǼ���ǰ�w�����ķֲ�����ɫ���^��ʾ����Ѫ���γɵķֲ���
�C�����������о��ɹ��_�l��һ���ע���ROS푑���ˮ���z�������ޏ��ж�-��ͻ�װY��B�µĽM��ȱ�p��ԓ���ϼ�����õĽM��ճ���Ժ������ԣ�������ROS푑����Լ��r��ļ���O��M2�;��ɼ����������T�����������߷������Ķ��p���ж�-��ͻȱ�p�^����w�S�����γɡ�ˮ���z�д����ă���ӻ��F�͌�ROS���е��������I֮�g�fͬ���ÿ���Ч��������h���ȶ���Ļ�����������ж����B�Ŀ�����������ͬ�rTA@Ag NPs��푑���ጷ��ܸ�Ч�l�]ˮ���z�Ŀ������������á����о����ж�-��ͻ�װY��B�½M��ȱ�p��ģ���У�ˮ���zͨ�^�p��ע��ɳ����� �ݲ�ճ���ڲ�Ҏ�t�Ą��ڃ��棬��߂����׃ϡ����������������䌦ȱ���Π��m�����ֲ����������ܷ��������a���������ܓp�M���Ȳ���С�g϶��Ч������Ť�Dȱ�p�^��ȱѪȱ���������h�����p�p�װY��ͬ�r���MѪ���γɺ��|�zԭ���e��������˿��@���ӿ쌍�����ж�-��ͻ��Ⱦȱ�ڵ������M�̡�
ԭ��朽�https://doi.org/10.1016/j.mtbio.2025.101856
- �|�A��W�����/ʷ��ꖽ����n�}�M��ACS AMI������֦����Ӱ����~�K�p���ټ{��ø�����[���h���{�ع��/������ 2025-06-19
- �Ĵ���W���Ʊ����ڡ����ɸ��о��T�F� AHM����ȫ��С���ӽ����Ƃ���h���{��ˮ���z�����ļ������ķֲ��ί� 2025-03-07
- �A�ƴ��_��/��˹��/�Ϸ��� Nat. Commun.�����ڿɽ���۶�Ȳ���ϵ��h���{���������ڷ��� 2024-11-15
- �����t���ǻ�tԺ�Մ�/�贺��/����Fꠣ�����ROS�|�lˎ��ጷ����ԵĿ�ע��ˮ���z���F�������Ϳ��{���w���fͬ�f�������������ί� 2025-04-15
- ���ִ�W��悌�����/�����ϲ�ʿ�F� Adv. Sci.�����������ܻ���ע��ˮ���z�p�p�װY���������M���Ժ����������� 2024-04-17
- ������W����淽��ڡ��ݿ�����ں������ั���ڈF� AFM���p�x���o�����p�ȹ��Ŀ�ע��ˮ���z����������P�Ĺ�ȱ�p�ޏ͎���������� 2024-03-27
