������y(t��ng)�ί��ֶΣ����䯟���Ĺ�Ч���ڸ��N��͵İ��Y�ί��еõ��J�ɣ��������������F���ص��ί����ܡ��[���Ͱl(f��)���D�ơ��о��������������ڽ���ݗ�մ̼����^�ָ߱��_MYC ���ס��@�N�������ޏ�DNA �p����������߀�������� I �ɔ_�� ��IFN-I�� ��̖ͨ·�������������ܺ��������ơ�
����Ҫ�c��
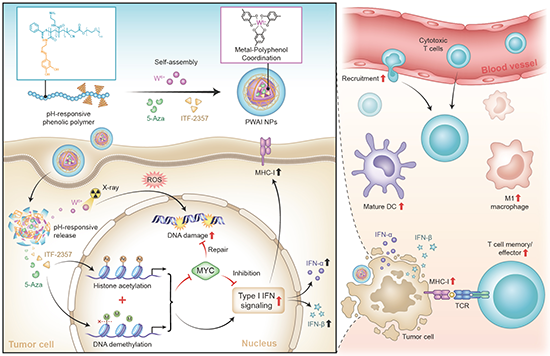
��1�����ⲿݗ���£�PWAI�ȵķů������u�x��ͨ�^�a������ROS�Ɖ����ٰ�������DNA朣�ͬ�r��ጷŵ�5-Aza��DNA���D��ø���Ƅ����c ITF-2357���M����Ó����ø���Ƅ����M�Ѕf(xi��)ͬ����������MYC�����ܓpDNA朵��ޏͣ��M���@�����M�ů����[������Ч����
��2���Mһ�����p���^�z���ί�ˎ���(li��n)��ʹ�ÿ������D�[��������IFN-I��̖ͨ·�����Ơ�B(t��i)�����@��� IFN-�� ��IFN-�� �����P����������ˮƽ����ԭλ���ٰ�С��ģ���У��@�N�ί��������l(f��)��ϵ�y(t��ng)�Կ��[������푑���������ͻ����ij��죬��������������ļ������ӛ�����͵��γɣ��Լ��[�����P���ɼ������������Ơ�B(t��i)������֧�֠�B(t��i)�����ߘO����
�����īI��
Wang, G., et al. Dual-Epigenetically Relieving the MYC-Correlated Immunosuppression via an Advanced Nano-Radiosensitizer Potentiates Cancer Immuno-Radiotherapy. Adv. Mater., 2024, e2312588.
DOI: 10.1002/adma.202312588
https://doi.org/10.1002/adma.202312588
- ���������ѡ������T��W����·�F��аl(f��)�����ͷů�ˎ�� 2023-03-20
- ���������w��ϯ�����n�}�M�ڽ���-�����λ�ۺ���̽ᘺϳ��c�����{�ط���ȡ����Ҫ�Mչ 2018-07-17
- ���ϴ�W���a������ AFM���۽��{��ˎ�����ȴ��y�} - �Գ�/�ň��p�����ӌ��FS�ͮ��|�Y�{��������[�������c������ 2026-03-26
- ����������W���d���ڈFꠡ�Adv.Healthc.Mater.���������p�����ص�pH푑��͟o�d�w�{��ˎ���Ч�ί���ϼ�����Ⱦ 2025-08-11
- �пƴ�������/�Y��F� Nat. Biomed. Eng.: ����һ��������NO��ͻ���[��Ѫ�ܻ���Ĥ���ϣ������{��ˎ�������f�� 2025-05-03
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m(x��)�ߏ��ȹ��-���������ѭ�h(hu��n)�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: ��(chu��ng)���͡��ø���{�ײ��� �� �I�������� 2025-07-20
�\���Pע�߷��ӿƼ�

- ���a���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)���h����...
- ��ˎ����Ч����������PMEC C...
- 2026����ߌ��Ї�����Ұl(f��)չ...
- �����IƱح300+���h��I(y��)�R��...
- �P���Ж|�����L���Ѓx�����{...
- �f����Ŀ �ذ��_�֣�2025�C...
- ICIE���H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_չ�ڼ����ۄ�������朄�δ...
- 9������Ҋ���£�AI��+���a...
- �P���e�k�ڶ�ʮ�����Ї����H...
- �۳Ǵ�Steven Wang���ڡ��^...
- �����ֿƴ��䏩/�ǫI�¡���...
- ���������ƾ��_���ڡ������i...
- �A�ƴ��T�ض����ڈF� Macro...
- �����������/���t(y��)������� ...
- ������ꐏ����ڈF� Matter...
- �������մ�/���� AFM���w�S...
- �A������߅�������w�i������...
- ���A��W���r�F� AFM���U�f...
- ���������x�����ڈF� Nat. ...
- �A�����������塢�V�|������...