�[��Ѫ���Ǽ{��ˎ���M(j��n)���[���M������Ҫ;������˼{��ˎ��ĸ�Ч�f���ںܴ�̶�����ه���[��Ѫ��ϵ�y(t��ng)��Ŀǰ���о���ʽ��Ҫ����1986���״�����ġ�����(qi��ng)�B�͜���Ч��(y��ng)����EPR, Enhanced Permeability and Retention effect����ԓ��Փ�J(r��n)�飬�[��Ѫ�܃�(n��i)Ƥ��(x��)�������Ǽ{��ˎ��B���[���M�������һ���������{��ˎ����������[��Ѫ�ܵĸߝB�ԁ���Խ�@һ���ϣ��Ķ�ֱ���M(j��n)���[�����|(zh��)��Ȼ�����R��ǰ���R���о��ĽY(ji��)�����@ʾ���{��ˎ��[�����f��Ч����Ȼ���M�����⡣ijЩ�о���(sh��)��(j��)�����������{���d�w�H�܌���s0.7%��ˎ����Ч�f�����[���M�����@һ�l(f��)�F(xi��n)�������l(f��)���Ɇ����Ƿ����������δ������J(r��n)�R�ęC(j��)�ƣ��@Щ�C(j��)�ƿ����ڷǃ�(n��i)Ƥ��(x��)�����ό�����K�˼{��ˎ���Ѫ����B��


�D1. �{���w�����[��Ѫ�����γ�Ѫ�ء�
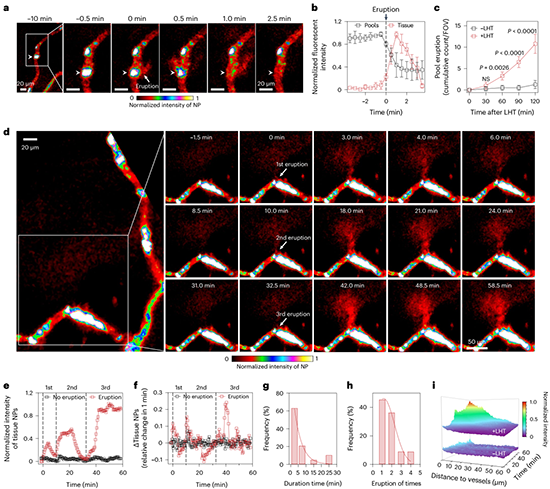
�D2. �����װY�T��(d��o)��Ѫ�؇��l(f��)������ס���ļ{���w��ጷŵ��[���g�|(zh��)�С�

�D3. ����Ĥ����ֹ�{���w���M(j��n)���[�������ϣ�ͨ�^�����װYͻ�ƻ���Ĥ���ϣ��T��(d��o)��ɽʽ���l(f��)��
ԭ��朽ӣ�https://www.nature.com/articles/s41565-023-01498-W
- �пƴ�������/�Y��F(tu��n)�(du��) Nat. Biomed. Eng.: ����һ��������NO��ͻ���[��Ѫ�ܻ���Ĥ���ϣ�����(qi��ng)�{��ˎ������(n��i)�f�� 2025-05-03
- �㽭��W(xu��)Ҧ�ˡ��n���܈F(tu��n)�(du��) Sci. Adv.������Ĥ����ˮ���z���M(j��n)��Ĥ�p�����ۻ����� 2024-12-23
- ���ϴ�W(xu��)���a������ AFM���۽��{��ˎ������(n��i)���y�} - �Գ�/�ň��p�����(q��)�ӌ�(sh��)�F(xi��n)S�ͮ��|(zh��)�Y(ji��)�{��������[�������c������ 2026-03-26
- ����������W(xu��)���d���ڈF(tu��n)�(du��)��Adv.Healthc.Mater.���������p�����ص�pH푑�(y��ng)�͟o�d�w�{��ˎ���Ч�ί���ϼ�(x��)����Ⱦ 2025-08-11
- ��������|/ꐾ��ɡ��۳Ǵ��T�����F(tu��n)�(du��) Adv. Mater.: ���-������s��������ڳ����dˎ���{��ˎ��ĸ�ͨ���B�m(x��)�����a(ch��n) 2025-02-12
- ������/���f/�Y�� JACS���l(f��)չ�ۺ���C֬�|(zh��)�d�wͨ�^�䷽��(y��u)������mRNA�����x�����f�͵Ķ����A(y��)�yģ�� 2026-03-03
- ��ʿ�m��W(xu��)��������ڈF(tu��n)�(du��) AFM��Һ�B(t��i)���ټ{���w���x�ܸ߷ֱ�ˮ���z3D��ӡ 2025-12-01
�\���P(gu��n)ע�߷��ӿƼ�

- ���a(ch��n)���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)���h����...
- ��ˎ����Ч����������PMEC C...
- 2026����ߌ��Ї���(sh��)�(y��n)�Ұl(f��)չ...
- �����I(l��ng)Ʊح300+���h��I(y��)�R��...
- �P(y��ng)���Ж|�����L���Ѓx�����{(l��n)...
- �f����Ŀ �ذ��_�֣�2025�C(j��)...
- ICIE���H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_չ�ڼ����ۄ�������朄�δ...
- 9������Ҋ���£�AI�(q��)��+���a(ch��n)...
- �P(gu��n)���e�k�ڶ�ʮ�����Ї����H...
- �п�Ժ���������F(tu��n)�(du��) Adv. ...
- �Ͼ����I(y��)��W(xu��)ë����/��҂�...
- �|�ϴ�W(xu��)�����/�����F(tu��n)�(du��) AF...
- �۳Ǵ�Steven Wang���ڡ��^...
- �����ֿƴ��䏩/�ǫI(xi��n)�¡���...
- ���������ƾ��_(d��)���ڡ������i...
- �A�ƴ��T�ض����ڈF(tu��n)�(du��) Macro...
- �����������/���t(y��)������� ...
- ������ꐏ�(qi��ng)���ڈF(tu��n)�(du��) Matter...
- �������մ�/���� AFM���w�S...
- �A������߅�������w�i������...