3��26�գ�Chemical Society Reviews �ھ��l�����A�пƼ���W�����WԺ�����Ҽ{��ˎ�﹤�̼��g�о����ė��������ڡ����Ӹ������Լ���贽�����ָ�����u��Փ��(Tutorial review) ��Influence of nanomedicine mechanical properties on tumor targeting delivery�����״Ό��{��ˎ�����W�����{�ز����c����á�ԭ�t��Y���������ʾ�{��ˎ�����W���܌����[��ˎ��˷��������ϡ����F����ݔ�͵���Ҫ���á�ԓ���±��x��ȷ������� (Inside front cover).
��������о��ˆT�l�F�{���d�w�܉���Ƃ��y����ˎ���ˎ�������W�Լ�����ֲ��������{��ˎ���[�������Բ����ͻ���ˎ������M���Ķ������á����������ڈF�������[���{��ˎ�������Եġ���á�ԭ�t�����ܵÄӣ�long circulation����ͣ���£�tumor accumulation�����@���deep penetration�����M��ȥ��cellular internalization���ͷŵó���drug release�������ڡ���á�ԭ�t�����������ڈF�ͨ�^�{�ؼ{���d�w���������|���������������λ���H��ˮ�ԡ�����늺ɵȣ������{��ˎ���ڸ����A�εĄ����W�О飻�����OӋ�ļ{��ˎ���ڄ����о����F�˸������Ŀ��[��Ч���Լ����͵Ķ������ã����P�о��ɹ��l����Advanced Science (2018, 2020)��Advanced Functional Materials (2020)��Nature Communications (2019)��Nano Letters (2018, 2019, 2019)��ACS Nano (2019)�ȌW�g�ڿ��ϡ�2019��5��20�գ����������ڡ���贽����c�S�����ں����������t�W����피��ڿ�Nature Biomedical Engineering�ϰl��Փ��The softness of tumour-cell-derived microparticles regulates their drug-delivery efficiency��ָ���[��������Դ�w�������W������ܛӲ�ȡ�׃������ͬ���@��Ӱ푼{��ˎ���ˎЧ�W�cˎ�ӌW�О飬��{��ˎ����OӋ�ṩ���²��ԡ�ԓ�ɹ����u�顰�A�пƼ���W2019��ʮ��W�g�Mչ�����õ����P�I��W�ߵĸ߶��J�ɡ�
�����@һ��Ҫ�о��Mչ�����Ӹ����ڡ������������n�}�M�����W피��C���ڿ�Chemical Society Reviews����Ո�����Y���l���P�ڼ{��ˎ�����W���܌�����á�ԭ�t�����A��Ӱ푵�ָ�����u��Փ�ġ����ȣ����º�����Ҫ�ؽ�B�����W�����ڼ{��ˎ���о��I���ѽ������Pע���S���������ˎN���õ����W�z�y���g���������˸�헼��g�ă����c�����ԡ�ͬ�r�����½�B�˾ŷN���õļ{���d�w����{�����z���ۺ����z�����A���ξۺ���ˢ����������{���z�ҡ������ԽM�b�z�ҡ��P���w�����{�����ݡ��s���{�������[��������Դ�w�������U����ͬ�{���d�w���W�����{�صķ�ʽ���@��{���d�w�����W�OӋ�������о��ṩ���Ѓrֵ�ą�����Ȼ��Ԕ����B�������˼{��ˎ�����W���܌��Lѭ�h���[����������B�������zȡ�Լ�ˎ��ጷţ�������á������A�����a����Ӱ푡�
-
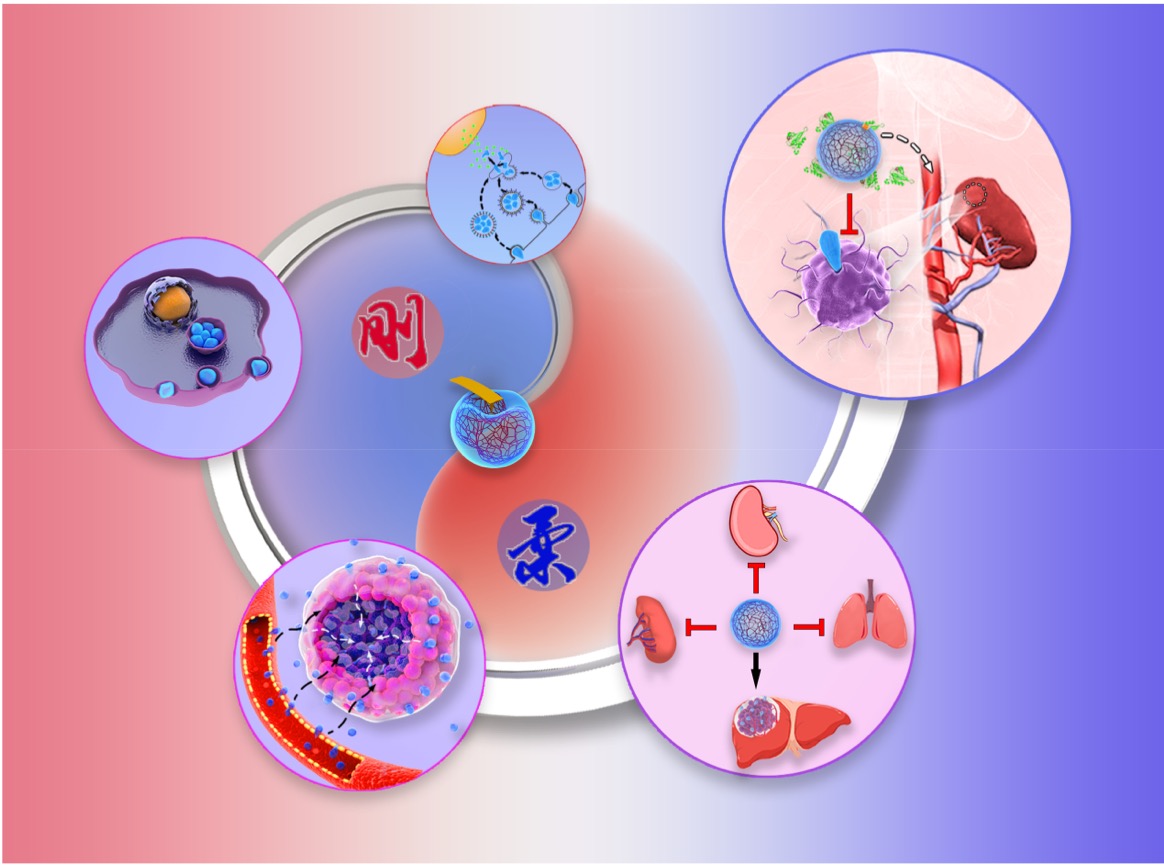
��һ�A�Σ�ܛ�ļ{��ˎ�������Ҏ�ܾ��ɼ����Ĕzȡ�����ⱻ�κ����ɼ���ϵ�y�;W���Ƥϵ�y��������F�Lѭ�h���и��ߵęC�����_�[����λ��
-
�ڶ��A�Σ�ܛ�ļ{��ˎ���cӲ����ȣ����A���ڸ������[����λ��������Ҫ�K���еĸ��������͡�
-
�����A�Σ�ܛ�ļ{��ˎ����и�������׃�����������Դ��^�[�������g���g϶���F��B��
-
�����A�Σ������о�����ܛ�ļ{��ˎ������ױ������zȡ�����ǣ������zȡ�^�̷dz����s��ͬ�r�ܵ����;���Լ��d�w�������|�����ص�Ӱ푣�����Mһ�����о���
-
�����A�Σ�ܛ�ļ{�����z���ھW�j�ܶ�ϡ�裬������ጷ�ˎ���������͵ļ{���d�w��δ���F�����@�����W������ه���ˎ�О顣
������¿��Y�����W���܌��{��ˎ��ݔ��Ч���Լ���K���[��Ч����Ӱ푣���δ��ֵ���Pע���������}�M����̽ӑ�������һЩ���еĽ�Q������
�A�пƼ���W�����WԺ���x��ʿ�����Ф���Լ���ʿ��Ӻ������ԓՓ�Ĺ�ͬ��һ���ߣ����������������Ӹ������Լ���贽����鹲ͬͨӍ���ߡ�ԓՓ�ĵõ��������c�аlӋ���Ŀ��������Ȼ�ƌW�����Լ��A�пƼ���W�W�gǰ������Fꠣ��������{���[���W�����Ŀ���Y����
Փ��朽ӣ�https://doi.org/10.1039/C9CS00575G
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- �пƴ�������/���/�Y��F� Science��ϵ�y��ʾ�߷����d�w���ϰl��ϵ�y������ĵәC�� 2026-03-20
- �㽭��W�������ڡ�����ܽ��ڈF� JCIS�����ڰ�ȫ�Ź������ʹ̼�푑�ˎ���f�͵ļ{������ 2025-09-09
- �|�ϴ�W�����۽����c������ Research�����ݞ�ģ��������Խ��ٶ���z������ˎ���f�ͺ��������[�������ί� 2025-07-31
