���գ��͵���W�߷��ӿƌWϵ�����������n�}�M��������ù��Ч��ጷ�һ��������NO�����w����������ˎ���[���ί����²�����ͨ�^���������ù��Ч���ļ{���d�w�͟����е�NO���w�Y(ji��)�ϣ���(g��u)����һ�N����NO�{�װl(f��)���������F(xi��n)�˽��t��������¾��ʿɿص�NOጷţ��ٽY(ji��)�ϰ�����ӣ�ԓ�{��ƽ�_����Ч�����[����λͬ�r���D(zhu��n)�[���Ķ�ˎ��ˎ�ԣ��Ķ���������Ч��������ˎ���[�����ί��ṩ����;������NO���P(gu��n)�ļ����ί�Ҳ������Ҫ���x��ԓ��������l(f��)���ڡ����M���ܲ��ϡ�(Advanced Functional Materials)�ϡ�
һ������(NO)�����w��(n��i)��Ҫ�Ě��w��̖���ӣ�����Ѫ��ƽ�����揈��ѪС��𤸽���װY�����߷�������(j��ng)���f�ȶ�N��������аl(f��)�]����Ҫ���á������������NO�@��w�����ί����P(gu��n)�������J����һ�N���͵��ί��ֶΣ����ЏV韵đ���ǰ����Ȼ������Ό��F(xi��n)NO�������w��(n��i)���\ݔ�Լ��ʴ_�Ŀ���ጷ���Ȼ��һ������y�}��
���˽�Q�@һ���}�����������ڈFꠘ�(g��u)���˪��صĽ��t���푑���NO�{�װl(f��)���������ù��ԇ���͟�����NO���w�Y(ji��)�ϣ���808 nm�Ľ��t��������£�ԓ�{��ƽ�_���Ԍ�������Ч�D(zhu��n)������ܣ��Ķ����M�����еĹ��wጷ�NO(�D 1)��
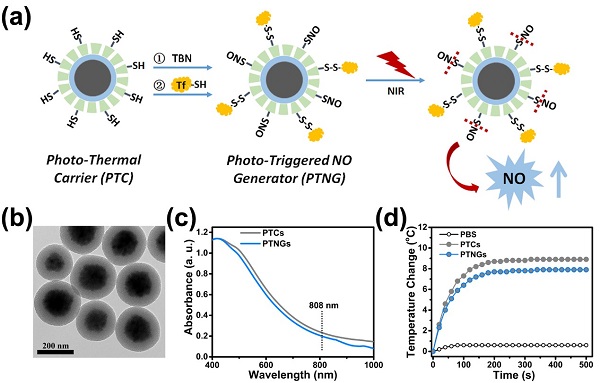
�D1. NO�{�װl(f��)�����Ę�(g��u)��ʾ��D
�������о��^���аl(f��)�F(xi��n)�� NO��ጷ��^�̌����t���������õ�푑������w����F(xi��n)�����@��off/on�О飬�����ü���۽��Mһ���ڼ���ˮƽ����C��NO푑�ጷŵ�����(�D2)��֮��������ԓNOጷ�ƽ�_������ˎ�Ͱ��Y���ί����������Y(ji��)�������a(ch��n)����NO�����܉�������ˎ�Ͱ�������P���ǵ��ױ��_���Ķ���Ч�������(n��i)����ˎ��ĸ�������������Ч��������ˎ���[��ģ�͵�������У��@һ�Y(ji��)�����ٴ��C�������M���[�����L�õ�����Ч���ơ��@�N���t���푑�ጷ�NO�ļ{��ƽ�_������ˎ���[��������NO���P(gu��n)�������ί�������Ҫ���x��

�D2. NO��ጷřz�y: (a) ���t���������(808 nm, 0.3 W·cm-2, 5 min), NOጷŵ�off/on�О飻(b) ���ßɹ�̽�DAFDA�z�y������(n��i)NO�a(ch��n)���ļ���۽��D��
����朽ӣ�http://onlinelibrary.wiley.com/doi/10.1002/adfm.201606398/full
- �пƴ�������/�Y��F� Nat. Biomed. Eng.: ����һ��������NO��ͻ���[��Ѫ�ܻ���Ĥ���ϣ������{��ˎ������(n��i)�f�� 2025-05-03
- �Ͼ���W�����n�}�M Sci. China Mater.��������늻��W�w�S���������ڌ��r���ʴ_�z�y�B��(n��i)һ������ 2024-02-05
- �㽭��WӋ����������F� ACS Nano��ͨ�^��(li��n)�|�l(f��)һ������ጷź���D�������F(xi��n)�����Ľ�(j��ng)Ƥ���W�����W���� 2023-08-27
- ���ϴ�W���a������ AFM���۽��{��ˎ������(n��i)���y�} - �Գ�/�ň��p�����(q��)�ӌ��F(xi��n)S�ͮ��|(zh��)�Y(ji��)�{��������[�������c������ 2026-03-26
- �㽭��W����Ⱥ/�㽭ʡ�����t(y��)Ժ���ƽ Angew��CD44���w�錧���D(zhu��n)���\�|�l(f��)�͵�����Ƕ���wCATCH���F(xi��n)�[��������⵰�Ľ� 2026-03-22
- �����������/���������������S�S Adv. Sci.���O���{(di��o)���c����ȱ�ݹ��̅f(xi��)ͬ������-����Ч�� - �����[���ί� 2026-03-01
�\���P(gu��n)ע�߷��ӿƼ�

- ���a(ch��n)���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)���h����...
- ��ˎ����Ч����������PMEC C...
- 2026����ߌ��Ї�����Ұl(f��)չ...
- �����I(l��ng)Ʊح300+���h��I(y��)�R��...
- �P���Ж|�����L���Ѓx�����{...
- �f����Ŀ �ذ��_�֣�2025�C...
- ICIE���H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_չ�ڼ����ۄ�������朄�δ...
- 9������Ҋ���£�AI�(q��)��+���a(ch��n)...
- �P(gu��n)���e�k�ڶ�ʮ�����Ї����H...