����W���ďV�����n�}�M���п�Ժ���M���g�о�Ժ�����L호��о��T����۴�W����\�t�WԺ�ąξS�ӽ����n�}�M��ǰ��ACS Biomaterials Science & Engineering�ϰl����һƪ��B������֧�ֹǼ������L��3D��ӡ���ϵ����£�3D-printed high strength bioactive supramolecular polymer/clay nanocomposite hydrogel scaffold for bone regeneration��Փ�ĵĵ�һ���ߞ��������ʿ��
ԓ��(N-��ϩ�����ʰ�����)��ճ��(PNAGA-Clay)�{�ͺ�ˮ���z���о��״Ό����S��ӡ�ߏ���ˮ���z֧�ܑ����ڹǽM���ޏ��С�

ˮ���z�V�����ڽM���������������ӽY���c�����w����Ȼ�ļ�������|��ECM�����ơ������ö��Ǟ��܇��Ļ���ṩ�Y���͠I�B��֧�νY���͠I�B�h����M����Ͷ�����������}��Ҫ�ܠ�Y�����Ǽ����t�ڶ�ײ����з�ֳ�ø��á�
���z��PNAGA����p�������ؚ��I���ã��x����ԓ���z�wϵ���������W���ܡ�����ӡ����֧�ܿ��Ա��S�⏝�ۣ������ܳ�����܇܇�w���뉺����Ѹ�ٻ֏�ԭò�����ܸ߉����֧�ܽY���������á�ͬ�r��ԓ���z֧����PBS��Һ���L�ڽ��ݺ����l�����@��Û�ҷ��������ã�ԓ���Ԍ������S��ӡˮ���z֧�ܺ���ò�ı������P��Ҫ��

���о�ͨ�^����3D��ӡ�ķ�ʽע�����z��ճ���w����һ�N�c�˹���Ȼ���ƵIJ��ϣ������ί���ͬ�̶ȵĹ��ۡ����ϵĻ��A�ǚ��I��ͨ�^���⾀�������ɸ����ķ��ӣ��@ʾ���߶��`��ęCе���ܡ��о��ˆTͨ�^���Ӳ�ͬ����ճ���w�������Ʋ��ϵĽY��������֮�g��ƽ�⡣

��ӡ�wϵ�м{��ճ�����������������������Mһ��������z֧�����W���ȵ�ͬ�r�����F�˳������ȴ�ӡ��ۺϵ����ڲ��������S��ӡ�������Ҵ�ӡ������S֧���ڹ����l�ۺ�ǰ�Y���������ã������l�����ݡ�����Ҫ�����w���w�⌍���������{��ճ���к��еĻ����x�ӣ����Դ��M�ɹǼ�����֧���ϵ���ֳ�Լ��ֻ�������Ч�ش��M�����ǽM����ȱ�p��λ����֧�܃Ȳ������L��
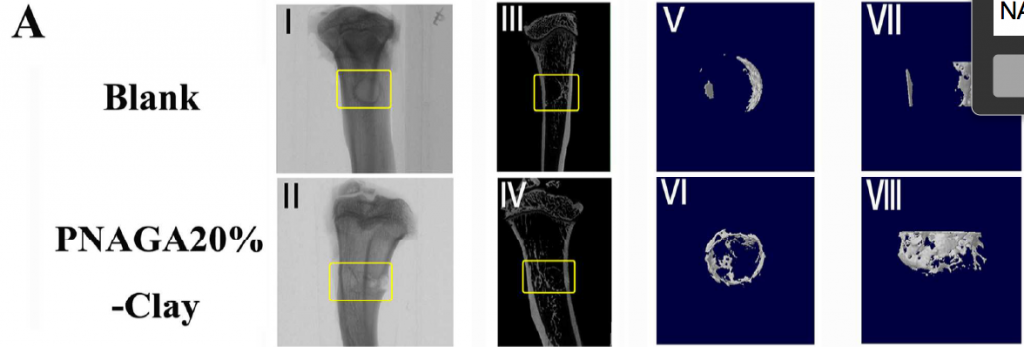
������֮�����I���w�c���N������ԟo�C�{�����ӵ�3D��ӡ���������ί����_�͂��w���ޏ�ȱ�p���˻��������d�M������֧���_���µ�;����
ԭ��朽ӣ�http://pubs.acs.org/doi/abs/10.1021/acsbiomaterials.7b00224
- �Ͼ����I��Wë����/��҂����ڡ��Ͼ���W�Ę��tԺ�O���ƽ��� AFM��ؓ�d�ɼ�������ˮ���z���D���w�S�� 2026-04-03
- �����ֿƴ��䏩/�ǫI�¡�����������ꐝ�/Ф�i��Nat. Commun.��: �nj��Q�H��ˮ���|�Y���ӿ���ˮ�Uɢ - �s��ˮ���z���F��Ч���ˮ�ռ� 2026-04-02
- ����i Adv. Mater.����x��-�л��i�Y����ע�䌧�ˮ���z - ���������ĽM��-������Ә��� 2026-03-21
- �ߴ����t���ڈF� Bioact. Mater.: �{��ճ��������3D��ӡ������ˮ���z����ֹѪ�c��Ⱦ�����ޏ� 2025-08-28
- �������Ʊ���Ժʿ/�������賯 AM������AIE���Լ{�ͺ�ˮ���z�Ŀɴ�������ʽ��Ϣ-���в��� 2024-03-23
- �Ϸ��t�ƴ�W���������/�¼�������W�СԪ���� AM������ճ���{���w���錧���[���F����/���߅fͬ�ί� 2023-12-07
