���|�����Թ����������y���R�����R������֮һ���@���HԴ�ڹ��|���Ɍ��µĹǽY��������ȱ�p��߀�c���۾ֲ�ʧ��Ĺ������h���������P����Ҫ�w�F�ڳ��m�������װY�c�����������ƹǼ������Ԯ������M���ɹǼ����ֻ��c�����ܓp���Լ�����Ѫ���γ��ϵK���@Щ������������γɲ���ѭ�h��������K�ǽM���������ޏ�������
���գ�ɽ�|��W�������ں��R���tԺ���B���������F��_�l�����ڹ��ޏ͵Ľ���-�ЙC�W�j�����N��ԓ�о�ͨ�^��������-�ЙC�W�j���ϣ����F�˿��ס���Ѫ�����ɼ��{��������/�γ�ƽ��Ķ��ػ��Գɷֵąfͬ�f�ͣ�ּ�ڏĶ�S���������������ľֲ��h�������������|�����Թ��۵��ޏ�Ч���ṩ�˸���ǰ�����²��ԣ��D1����
2025��12��4�գ����P�о��ɹ��ԡ�Engineering of Metal�COrganic Networks as Band-Aid for the Repair of Osteoporotic Bone Fractures�����}�l���ڡ�ACS Nano���ϡ�ɽ�|��W���W�c�����WԺ�����������R���tԺ���B��������ԓՓ�ĵĹ�ͬͨӍ���ߣ�ɽ�|��W���W�c�����WԺ��ʿ��κ�B�y���R���tԺ��ʿ���������ԓՓ�ĵĹ�ͬ��һ���ߡ�

�D1. PZnCaE�����N�ί����|�����Թ��۵�ʾ��D����a��PZnCaE�����N���Ƃ������D����b��PZnCaE�����Nͨ�^�����������������ƹǼ������ԡ��{�����߲����MѪ�����ɵ����ÙC�ơ�
�о��Fꠌ������|���ɽ���ˎ�ﰢ������c��ALN����֦�����Ҷ�����PEG���ϣ��γɿɽ���ľW�j�Ǽܣ��ɳ��mጷ�ALN�Ծ��������^�ȵ��ƹǻ��ԡ��S�������\�x�ӣ�Zn2+�����}�x�ӣ�Ca2+���cALN����Ȼ��ӵ���λ���ã�����N���ܽM�����ϵ��DŽ����N�У����H�����˲��ϵ����W���ܣ�߀����Ч���M�ɹǷֻ���Ѫ�����ɡ���ӽM�ֿ��������������������װY���������ޏ��к���M1�;��ɼ����O���������M2�ͣ��Ķ����F���������{�������w���ԣ��@����N�����DZ��ӵ���������һ����ͬ�r���_�������ƹǡ����M�ɹǡ��̼�Ѫ�ܡ�ƽϢ�װY���Ĵ�ָ��������{��ƽ�_��
ԓ�о����ý����x�ӣ�Zn2+/Ca2+���cALN��EGCG֮�g��Ȼ����λ���ã�ͨ�^���εĻ�ϡ��x�ļ����γɷ����Ľ���-�ЙC�W�j���@�N����Ч���Ƃ䷽�������ˏ��s�Ļ��W�ϳɣ��������õ��D�������������N�ڽ����^���У��ܰ��衢���m��ጷ�ALN��Zn2+��Ca2+��EGCG�ȶ�N���Գɷ֣�ģ�M����Ȼ���ޏ��^���в�ͬ�A�ε�����W�����F���ί����ӵ�������Ͷ�������о���Խ�ˆμ������ɹ�-�ƹǡ�ƽ���{�أ����뵽�˹����ߌWǰ�ء�ͨ�^EGCG�{�ؾ��ɼ������ͣ����������Ɖ��ԡ��h���D���鿹�ġ��ޏ��ԡ��h�����ĸ���Ӵν�Q�˹��|���������ϵĺ����ϵK��
ԓ�о�ͨ�^ϵ�y�IJ����Ƃ��c�������w�⼚�����w�Ȅ���ģ����C��ȫ���u�������аl�ĹDŽ����N��PZnCaE����Ч�����D2-7�����о���������������R��X�侀��������V�ȱ����ֶ��C���˲��Ͼ��з����Ķ�Y�����A�ڵĻ��W����������W�yԇ����Û�c���⌍��Լ��w��ጷ�����������ԓ���Ͼ������õęCе���ܡ��ɿصĽ������ʺ�ALN��Zn2+��Ca2+�ij��mጷ��������D2�����w������W����Mһ����ʾ�DŽ����N�������õ����������ԣ�����ȡ�����@�����M�����g���|�ɼ����ijɹǷֻ���ALP���ԡ��}�Y���γɼ����P����/���ױ��_���{���������ƹǼ����ֻ���TRAPȾɫ��Ԝp�ټ����P��־�����{�������M��Ě�o�}��Ƥ�������w���c�ɹܣ�Ѫ���������P����/���ױ��_�������������T�����ɼ�������M2���͘O����CD206���_���ߣ��װY���ӷ��ڜp�٣����D3-5�����ڹ��|���ɴ����B��ȱ�pģ���У�ֲ��PZnCaE�����N8�ܺ�Micro-CT���S�ؽ������������@ʾ����ǵV���|�ܶȣ�BMD�������w�e�֔���BV/TV����ָ���@�����ڌ��սM�������νM�ֲ��ϽM���M���WȾɫ��H&E��Masson���^�쵽���������¹��c�zԭ�γɣ����ߟɹ�Ⱦɫ�Mһ���C��ȱ�p�^���и����ijɹǣ�COL1��BMP2������Ѫ�����ɣ�CD31����̖���@����M2�;��ɼ�����ARG1���ۼ����D6-7����ԓ�о����H�ṩ��һ�N���R���D�������Ĺ��ޏͲ��ϣ���չʾ��һ�N�������OӋ-�h���{��-�M���������fͬ���ԡ�ͨ�^������λ�M�b���F���ػ��Գɷֵĕr��ጷţ�����x�ԹDz����ޏͲ����_�l�ṩ����˼·��

�D2. PZnCaE�����N���Ƃ��c������������a����ͬ��̈́����N��SEM�D��b��PZnCaE�����N��Ԫ�طֲ��D����c��PZn��PCa��PZnE��PCaE��PZnCaE�����N�����쑪��-��׃��������d��8-arm-PEG-ALN��PCa �� PZn �����N��XPS�V�D��������e���γɄ����N�������ʾ��D����f����Û������������g���w�Ƚ���ɹ�����ԈD��h���w�ȶ���������������i��ALN��Zn2+��Ca2+���w���۷eጷ�������
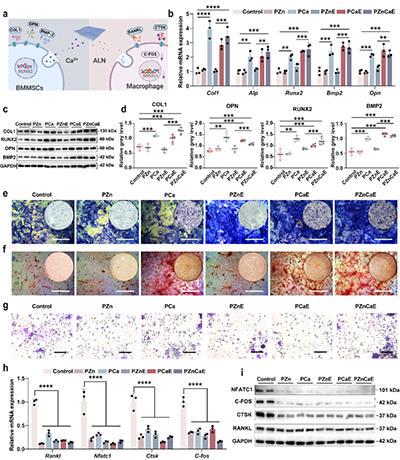
�D3. PZnCaE�����N�{��BMMSCs���w��Ƿ��B�О�����a��PZnCaE�����Nጷ�Ca2+��ALN�Դ��M�ɹǼ����ֻ��������ƹǼ���������ʾ��D����b���ɹ����P����mRNA���_ˮƽ����c��d���ɹ����P���ױ��_ˮƽ�������Y������e��ALPȾɫ�Y������f�����ؼtSȾɫ�Y������g��TRAPȾɫ�D��h���ƹ����P����mRNA�����_ˮƽ����i���ƹ����P������WB������

�D4. PZnCaE�����N��Ѫ�������{���c���ɼ����O�����w���{���о�����a��PZnCaE�����N�{��Ѫ�����ɺ����߷�����ʾ��D����b��Ѫ�����P����mRNA���_ˮƽ����c,d��Ѫ�����P���ױ��_ˮƽ�����������Y������e����ͬ̎��l����HUVECs��Ѫ��������������f���װY���P����mRNA�ı��_ˮƽ����g,h����ͬ̎������CD206��iNOS��ARG1�ĵ��ױ��_ˮƽ�������Y������i,j�����ɼ����O�����ͼ������Y����

�D5. ͨ�^���ɼ����O���{�سɹǺ�Ѫ�����ɵ��w���о�����a�����þ��ɼ����O���{�سɹǺ�Ѫ�������Č�����̡���b����ͬ̎���M�ɹ����P���������_ˮƽ����c,d���ɹ����P���������_ˮƽ�����������Y������e,f��ALP�����ؼtSȾɫ����g���w��ɹ���������h����ͬ̎���MѪ�����P����mRNA�����_ˮƽ����i����ͬ̎���MѪ�����P���ױ��_ˮƽ�Ķ����Y������j�����þ��ɼ����O���{�سɹǺ�Ѫ�����əC��ʾ��D��

�D6. PZnCaE�����N�{�ع��|���ɹ����ϵ��w���u������a��ʹ��PZnCaE�����N�ί������ϵ�ʾ��D����b����ֲ��0��4��8�ܵ����SMicro-CT�D������c,d����4�͵�8��Micro-CT������������e����8��ȱ�p�^��H&E��MassonȾɫ��

�D7. �w�ȳɹ����á����߷�����Ѫ�������u������a��ȱ�p�^�� RUNX2 �� OPN �����߽M��Ⱦɫ�D��b,c��ȱ�p�^�� BMP2����c,d��COL1�����ߟɹ�Ⱦɫ�D��Ͷ�����������f,g��ȱ�p�^��iNOS��ARG1�����ߟɹ�Ⱦɫ�D��Ͷ���������
�C�����������о��ɹ��_�l��һ�N���ڽ���-�ЙC��λ�W�j�Ķ�ܹ��ޏ�֧�ܡ������H�H��һ���Y����������һ���܉�ӑB푑����������ֲܾ������h���ġ�����ϵ�y����ͨ�^�fͬ�{�ء��ƹ�-�ɹ�-Ѫ��-���ߡ��@�Ĵ��P�I�h����ԓ�����N��Ч���D�˹��|�����Թ�ȱ�p�IJ����l�������F�˸��|���Ĺ��������@헹������ί����|�����Թ��ۼ������y���Թ�ȱ�p�ṩ��ȫ�µIJ����OӋ˼·�������о������õ�������Ȼ�ƌW�����c�������c�аlӋ�����Ŀ���Y����֧�֡�
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/acsnano.5c15619
- �A�|���������x�����n�}�M AFM�����ڷ����ЙC-�o�C�����W�j�������������ڹ��ޏ� 2025-11-04
- �㽭��W�w�h�_�F� AFM: �����ݶȽY��ˮ���z������ܛ���ޏ� 2025-10-15
- �{����Դ�������֡�����/�����ǻ�tԺ�����١�� Adv. Mater.���Cе-�x���ˮ���zͨ�^��Դ������늴̼����Mܛ������ 2025-09-23
- �|�A��W�������о��T/ʷ��ꖽ��ڈFꠣ������Q���ט�������f�Ͳ��}����ø���ڹ��P���Ŀ���ܛ�DZ��o�ί� 2025-06-13
- ���������ڈF� Bioact. Mater.����ˎ���f��ϵ�y"������-����-����ϵ�y���o"��λһ�w�fͬ����ʹ�L���P�����ί� 2025-06-04
- �����t���ǻ�tԺ�Մ�/�贺��/����Fꠣ�����ROS�|�lˎ��ጷ����ԵĿ�ע��ˮ���z���F�������Ϳ��{���w���fͬ�f�������������ί� 2025-04-15
- �п�Ժ�������MԺ�w����/�˺Ʋ�/߅�����F� CEJ��ؓ�d⋓��s������Բ����Ŀ�ע��ˮ���z���û��������������ί��������Ԅ��� 2024-01-31
