�A�������삥���Ͽƴ�����Դ�����������w���� Nat. Commun.���{��������Ч���錧�����w�ȾۺϷ���

�����w�ȟo�r�o�̲��M�������N���ӵĻ��W���������磬����ϳɶ��ǡ������|�ͺ��ᣬ�@���H�����������w����ĸ��N�����ɷ֣�Ҳ�x���������w���N���ܣ����{���������M�̡���ֹĿǰ���ѽ���һЩ��Դ�Ի��W�����ɹ����w�Ȱl�������������c���������D�ƚ仯��Ó�����o���Ȍ��F�����w�Ⱥϳɟɹ�̽ᘣ�����ˎ��ۺϷ�����һ�N�ϳɶ�N���ӣ������{�ش���ӻ�������ձ鷽�������Ԟ�ƌW�����⣬�������{�����������ṩ�o���ܡ�Ŀǰ��һЩ���ڳ����Ӻ��r�ľۺϷ������������w�Ȱl���������˶�N���ܲ��{�����ﷴ�����������w�Ќ��F�˹��ۺϷ������R��һЩ���H���y��1��ͨ����Ҫ�\ݔ�ߝ�ȵĵ��2�������w���ձ���ڵĻ������|�ʹ��x�a����ܕ����ƾۺ��^�̣�3�������ۺϷ�����Ҫ�~��Ĵ̼��������������⣬�����x�ӵȣ�4��Ŀǰ�w�Ⱥϳɵľۺ��﹦��߀���^���ޡ�

�D 1. �����w�ȾۺϷ���ʾ�������ü{�����������������w�гɹ����F��Դ�Թ�ۺϼ���Դ�������ۺϵ�ʾ��D��
ᘌ��@Щ���}���A��������W����ƌW�c���̌WԺ�삥�������Ϸ��Ƽ���W����Դ���ں��¼�������������W�w����������ͬ�OӋ���ü{�����������������w�гɹ����F��N�ۺϷ����İl�����D1�����{�����ṩ��һ�N���ĭh����ʹ�Æ��w��ǻ�w�Ⱦ����^�ߵľֲ���ȣ�����ˆ��w��ײ��Ч�ʣ����Ա������ߝ�ȵĆ��w���Ķ����͆��w�ĝ��ڶ��ԡ��{����Ҳ����w������һ���[�صĭh�������Խ��ͻ������|���ھۺϷ�����Ӱ푣����ڶ�N�ۺϷ������w�Ȱl����
����Դ�ԵĹ�ۺϷ�������������ϩ�����c��NaSS���ڹ����l���Ĵ����£��S�����Օr�g�����L����ۺϷ����l�����ɹ⏊�����������������ݰ��dNaSS�����l������ۺϷ����ٶ�������2.7�����քe�������ݺ͛]�����ݵ�NaSS���뵽4T1�����У�����4С�r���M�й��գ��l�F�����ݽM�ğɹ⏊�����ӱ�����o���ݽM�ɹ⏊�����ӱ�����2.9�����f���˼{���Ҍ��ڼ����Ⱦۺ����������ã��D2����

�D 2. �{���������Խ錧����Դ�Թ�ۺϷ�����
������Դ�Դ̼���������x�ӣ��⣬��ȣ��팍�F�w�Ⱦۺ��ڌ��H�����ж������ޣ���Դ����̖�����^�����䣬��pH�����Nø��t���F���˘O�������������ݰ��d�����^������ø��HRP���ͱ����������Ԍ��F�^������푑��ă�Դ�Ծۺϣ��D3�����о��l�F�����ڲ�ͬ�ı������������݅f���µľۺϷ����������@���ڛ]�����ݵľۺϷ������ʡ�ͬ�r�����������r�ļ�����������ɔ_��r�������ݵľۺϷ��������˸��ߵķ������ʣ��C���˼{���Ҟ���w�ṩ��һ�N�����x�ĭh���������˾ۺϷ������ʣ�Ҳ�ṩ��һ���������ľۺϭh����

�D 3. �{���������Խ錧�ă�Դ�������ۺϷ�����
���@Щ�����У�ADPAH@AOT��푑�H2O2���ڽ��t����^��NIR-II�����F�������@�����գ��Mһ�����о��l�F��������^�õ�NIR-II�Ĺ������ܡ�ͨ�^�c�[�������������l�F������T���[����������ԭ��������ICD�������M��ͻ����컯���������߷������D4���������[��̎���^���_��H2O2��ʹ��ԓ�wϵ�Н�������ɼ����NIR-II��������ί����Mһ���أ��ڲ��}����ø�����[����������|�ąf���£�ADPAH@AOT��С���w�����M��ICDЧ�������M�˘�ͻ����ij��죬�Mһ��������T�����Ľ���������������푑��������H�����ԭλ����Ҳ�Mһ�����������h�������@������Ч�Ĺ�������ί�Ч�����D5����

�D 4. ADPAH@AOT��������ԭ�����������M��ͻ��������������
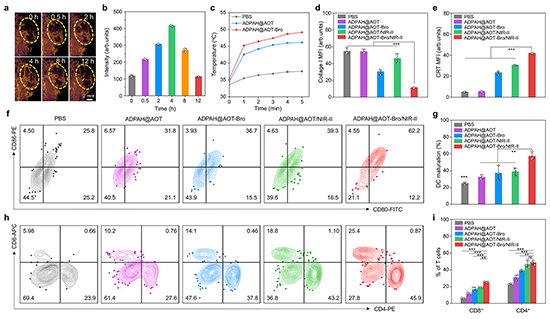
�D 5. ADPAH@AOT푑��[��̎H2O2�ۺϷ����İl�����伤���������ί��ı�����
�������P�ɹ�����Nanocompartment-confined polymerization in living systems�����}�l���ڡ�Nature Communications���ϣ�ԓՓ�ĵ�һ���ߞ��¼�������������W��ʿ������ͨӍ���ߞ��A��������W����ƌW�c���̌WԺ�삥�������Ϸ��Ƽ���W����Դ���ں��¼�������������W�w�������ڡ�ԓ�о��õ��ˇ�����Ȼ�ƌW������Ŀ֧�֡�
ԭ��朽ӣ�https://www.nature.com/articles/s41467-023-40935-1






