���ڣ�����W�����WԺ�����½����n�}�M�ڳ������ԽM�bDNA�{��ϵ�y�����[���������W�ͻ���fͬ�{�ط���ȡ�����Mչ�����P�ɹ��l���ڻ��W�I������ڿ�Angewandte Chemie�������û��W��������W�����WԺ���P���������о����������鹲ͬ��һ���ߡ��о��õ�������Ȼ�ƌW����ȵ��Y��֧�֡�

�����ȵ�����߀ԭƽ���ǾS�������������x���ܵ���Ҫ���A�����[�������ȣ����ڻ���ͻ׃��ɴ��x������������ˮƽ��������������ͨ�^���̼��¸������_���������ֵ����ɼ����p����Nrf2���{������߀ԭƽ����P�I�D����ӣ����{�ؼ����ȶ�N������ø�ı��_�����û���ˎ���{���[��������Nrf2�ı��_���܉������[�������������������������L����һ�N�O�ߝ������[���ί����ԡ�����_�l��ȫ��Ч�Ļ����f���wϵ�����F�c�����ί������ąfͬ������ԓ���Ԍ��Fͻ�Ƶ��P�I��DNA��һ�N�������������ӣ����з����R�e�ԡ����пɾ������Լ����{��������ԣ��ҿ��c�����wϵ��ό��F�༉�νM�b�����ʘ���������DNA���ܲ��ϣ��ں���ˎ���f���I��չ�F�����õđ���ǰ����
�����½����n�}�M������һ�N�������ԽM�bDNA�{��ϵ�y��ͨ�^���W�ͻ���fͬ�{�������[���������������������F�ˌ��[���ĸ�Ч���ƺ��ί����D1�����������Ⱥϳ��˃��H�����ѣ�TeEG2�������cMn(II)��λ�γɏͺ��Te/Mn����Te/Mn�cđ�̴����DNA���M�b���ɾ�����D�����Ե�DNA�s���{���z�����^���ڼ{���z�������DNA�������l��|�l�l��DNA��H1��H2���M�м��Qʽ�s���ʽ������C-HCR�������F�{���z�������ϵ�DNA�W�j�ӑB�M�b���l��H2ĩ�����ATP�m���w��ͨ�^�A�����a�䌦�c����ˎ��siNrf2�B�ӣ����FsiNrf2��DNA�W�j�ĸ�Чؓ�d��TeEG2���г�ɫ�Ħҹ�����������ɴ��M��ӏ�Mn(II)��H2O2���D�ƣ������Mn(II)����D�����Ĵ����ԣ����[�������Юa�������߶���?OH�����F���[�������Ļ��W�{�ء�ͬ�r�����[��������ATP�������£�DNA�W�j�е�ATP�m���w�l��׃�������FsiNrf2���خ��Կɿ�ጷţ����{�D�����Nrf2�������P������ø�ı��_�����F�������Ļ����{�ء��w����w�Ȍ��������������{�ؿ��c���W�{�fͬ�����@�������[�������������������Ķ������[�����������L��
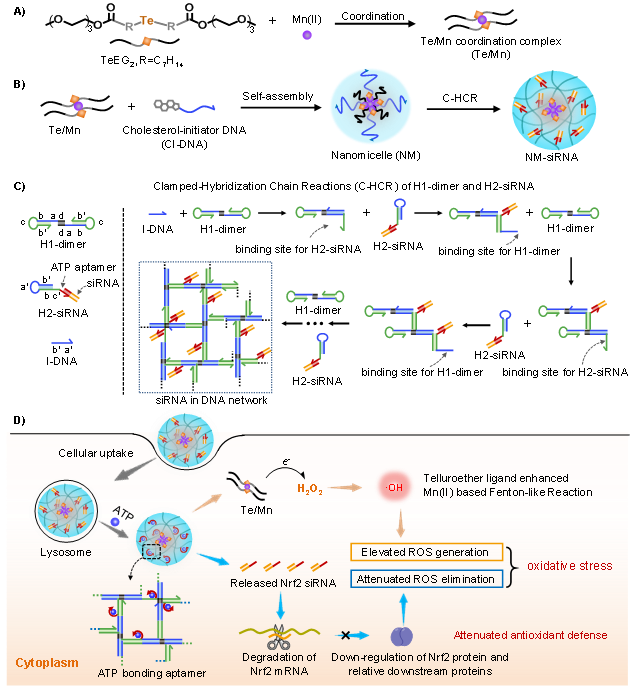
�D1. �������ԽM�b DNA �{��ϵ�y���F�[���������W�ͻ���ąfͬ�{�ء�A) ��B) �������ԽM�bDNA�{��ϵ�y��������ʾ��D��C) DNA���M�b���FsiRNA��Ч�b�d��D) ������siRNA�خ��Կɿ�ጷţ����F�[�������Ļ��W�ͻ���fͬ�{��
ԓ��������ij������ԽM�bDNA�{��ϵ�y�������[����������������И˵��ί������ṩ����Ҫ�IJ��ϻ��W���A�������ƄӾ����t���İlչ��
ԭ��朽ӣ�https://onlinelibrary.wiley.com/doi/abs/10.1002/ange.202111900
�������n�}�M����������DNA���о��������۽�DNA���﹦�ܲ��ϻ��W�M�b�c�������죬���������������ͼ����ί����n�}�M��퓣�http://yanglab-dna.com/
- �A�����γ��n�}�M��Nano Lett.�������ھۺ����ɳ��^���{�؟o�CѨ���ԽM�bͨ���x�ӂ�ݔ�����W�Ć��x�ӌ��w�OӋ���� 2023-03-22
- ���K�ƴ����/ʩ������Ceram. Int.�����h���Ѻ��ͳ������ԽM�b�ϳ�S���s���Ķ�ܠ�ۺ��ﵪ��̼��������a�� 2023-03-13
- ���չ��I��W���o�����ڈFꠡ�ACS AMI���������ӹ���׃ɫ���ϵ������о��ɹ� 2023-01-06
- ��܊܊�t��Wţ���Ƚ��ڈF� ACHM�������Y���fͬ�����{�ص�DNA-�zԭ���ό��F�����o������? 2025-08-19
- �X�ϴ�W/�¼��¿Ƽ��о��ֵ� Nat. Commun.���_�lDNA���ɻ�����ѭ�h�������� 2025-08-15
- ����W/������W Sci. Adv.�����ڹ����������ĸ�����DNA�����惦�S�C�L�����g 2025-06-21
- ��h��Wꐳ���/���� Natl. Sci. Rev.���ɻ�������z����������ˮ���z늽��|�����ɳ��m�������\����늳� 2025-08-11
