ͨ�^(gu��)���W(xu��)��������������(d��ng)��M��������ȥ����Ҫ��(x��)���ɷֺ�����ԭ�ԫ@�õ�Ó��(x��)�����|(zh��)֧���ѳɞ�Ŀǰ�M�������о��ğ��c(di��n)���@Щ֧�ܿ����^�õر���ԭ�M�������ٵļ�(x��)������|(zh��)���׳ɷ֡��������Ӻ���Ȼ�����S�Y(ji��)��(g��u)��������˹��ϳɲ��Ϻ���Ȼ�Ć�һ�ɷֲ�������ֲ��(x��)��������߃�(y��u)��(sh��)���������^��߀ԭ�M���ܓpǰ���h(hu��n)�������д��M(j��n)��(x��)��ճ������ֳ�ͷֻ�����������Լ������オ������ԣ�������Խ��(l��i)Խ��Ĉ�(b��o)���C�������﹦���c�ޏ�(f��)Ч�����нM���خ��ԡ�Ŀǰ���M����(l��i)Դ��Ó��(x��)�����|(zh��)֧�����ڽM�������I(l��ng)���ѽ�(j��ng)�õ��dz��V���đ�(y��ng)�ã��������K��Ĥ��Ѫ�ܡ�Ƥ�w��������ܛ�ǡ���ܡ��Ρ��܇���(j��ng)�ȣ����в��֮a(ch��n)ƷҲ�ѫ@��ʳˎ�O(ji��n)�ֵ�����(zh��n)����(y��ng)���ڲ�ͬ�R���m��(y��ng)�Y���ί�������������ϡ�ܛ�M���ޏ�(f��)�����K��Ĥ�ÓQ�ȡ��M��Ó��(x��)�����|(zh��)�ѵõ��������t(y��)�W(xu��)�I(l��ng)��ďV���J(r��n)ͬ�c��ҕ���@��ϱ����(l��i)Դ��ȱ���y���������a(ch��n)�ͼӹ��Ć�(w��n)�}��Ȼ��(y��n)�������⣬Ŀǰ��(du��)��Ó��(x��)�����|(zh��)�ĽM�ɳɷ��c�M���خ���֮�g�P(gu��n)ϵ���J(r��n)�R(sh��)�Էdz����ޡ�
��ɽ��W(xu��)���ϿƌW(xu��)�c���̌W(xu��)Ժȫ��Ƽ���ڡ����������n�}�M�����(l��i)ͨ�^(gu��)һϵ�в��όW(xu��)�ֶΌ���(j��ng)�M�����܇���(j��ng)�ͼ���ȣ���(l��i)Դ��Ó��(x��)�����|(zh��)֧���D(zhu��n)�����ע�䡢�ɼӹ��ļ{���w�Sˮ���z���о��@ʾ���c�����(l��i)ԴÓ��(x��)�����|(zh��)ˮ���z��ȣ��܇���(j��ng)��(l��i)ԴÓ��(x��)�����|(zh��)ˮ���z(decellularized peripheral nerve matrix hydrogel��DNM-gel)���w�����B(y��ng)������(j��ng)��(ji��)�r(sh��)���ɴ��M(j��n)�����Sͻ�����ʻ�������ͻ�|���γɣ��@һ�l(f��)�F(xi��n)�C��(sh��)ԓ����Դ�Բ��ϳ�������Ȼ��(x��)������|(zh��)�ĸ���������⣬߀�������_�ĽM���خ��ԣ�Adv. Funct. Mater. 2018, 1705739��������DNM-gel�����ȡ��Y(ji��)��(g��u)���o늼��z�w�S����(sh��)�F(xi��n)����(j��ng)�Sͻ��ʩ�f(w��n)��(x��)���ąf(xi��)ͬ���ٶ������L(zh��ng)��ACS Appl. Mater. Interfaces 2019, 11, 17167?17176������������x���g(sh��)�Ƃ�Ķ���v��ͨ��DNM-gelˮ���z��(j��ng)��(d��o)�ܣ��ژ�Ӵ���������(j��ng)ȱ�p�����M(j��n)�������ޏ�(f��)�����������@�����кܺõđ�(y��ng)��ǰ����Acta Biomater. 2018, 73, 326 �C 338��Mater. Sci. Eng. C 2020, DOI: 10.1016./j.msec.2020.111791��������Ó��(x��)�����|(zh��)�����к����S���ĵ����ǣ��������õĽY(ji��)�ϲ�������L(zh��ng)���ӵ����������p�����ӵ������£�NGF��VEGF�����w���^�쵽��(j��ng)�w�S�cѪ�ܾW(w��ng)�j(lu��)�ąf(xi��)ͬ�������w��(n��i)�^�쵽���M(j��n)Ѫ�ܻ�����Ч�����(j��ng)���ܵĻ֏�(f��)��Tissue Engineering Part A 2020, DOI: 10.1089/ten.tea.2020.0227����
����ԓ�F(tu��n)�(du��)ͨ�^(gu��)���όW(xu��)���D(zhu��n)䛽M�W(xu��)�����|(zh��)�M�������ȶ�N�ֶΣ���(du��)Ó��(x��)��������|(zh��)ˮ���z��decellularized spinal cord matrix hydrogel��DSCM-gel����DNM-gel�M(j��n)���˾��w�ķ������^���о��l(f��)�F(xi��n)���ɷNÓ��(x��)�����|(zh��)ˮ���z�������c��(x��)������|(zh��)��Ƶļ{���w�S�Y(ji��)��(g��u)����DSCM-gel�Ŀ�϶�ʺ��w�Sֱ���Ը���DNM-gel������(j��ng)��/�漚(x��)����neural stem/progenitor cell��NSPC��������Ó��(x��)�����|(zh��)ˮ���z���M(j��n)�����S���B(y��ng)���l(f��)�F(xi��n)DSCM-gel��������NSPC�Ĵ���ֳ���w�ƣ������܉���M(j��n)NSPC����(j��ng)Ԫ��ֻ����D1����
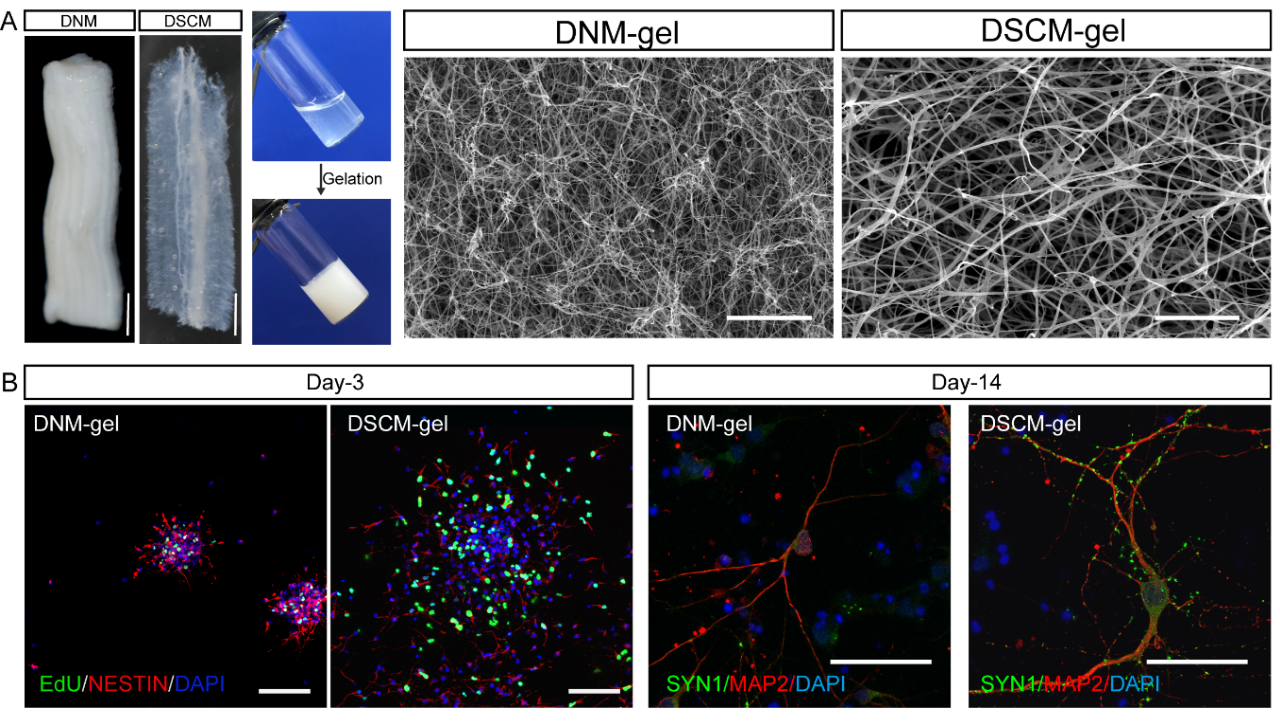
�D1. Ó��(x��)�����|(zh��)ˮ���z���Ƃ��cSEM������ˮ���z�е����S��(x��)�����B(y��ng)�C��DSCM-gel�����@�����M(j��n)��(j��ng)�ɼ�(x��)����ֳ���w�ƺ�����(j��ng)Ԫ�ֻ���������
�Y(ji��)��RNA-Seq���_(d��)�V�y(c��)���g(sh��)��������Ϣ�W(xu��)�������l(f��)�F(xi��n)DSCM-gel���S���B(y��ng)ģʽ�����@���M(j��n)NSPC��(j��ng)Ԫ��ֻ��Լ�������(j��ng)Ԫ�ij��졣�D(zhu��n)䛽M�����M(j��n)һ��������DSCM-gelͨ�^(gu��)�{(di��o)��(ji��)������ (integrin) ����Itg��2��Itg��9��Itg��9���ı��_(d��)�V�Լ�AKT/ERK���P(gu��n)��̖(h��o)ͨ·��(l��i)�{(di��o)��NSPC���О飨�D2����

�D2. DSCM-gel�{(di��o)��(ji��)�����ػ���ı��_(d��)�V��AKT/ERK���P(gu��n)��̖(h��o)ͨ·�{(di��o)��NSPC���О顣
�����|(zh��)�M�W(xu��)����������DSCM�M���خ��Եļ�(x��)������|(zh��)���ף����ճ�B���ף�LAM�������쵰����(TNC)��һЩ���������L(zh��ng)����(FGF2)���܅��c���@Щ�{(di��o)�أ��D3�������⣬�w��(n��i)�u(p��ng)���C��(sh��)��DSCM-gel�������ȫ�M���p����ă�(n��i)Դ��NSPC��ļ�����Sͻ�����ṩ�˺��m���h(hu��n)����
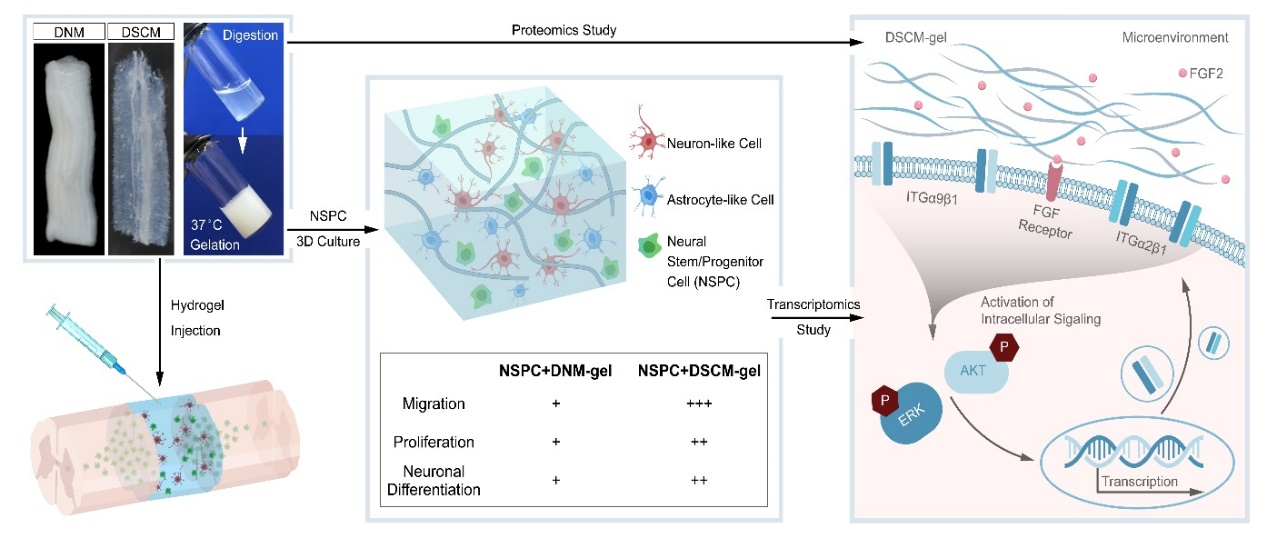
�D3. Ó��(x��)��������|(zh��)ˮ���z���Ƃ估����Ч���M(j��n)��(j��ng)�ɼ�(x��)����ֳ���ֻ�����(j��ng)Ԫ��ֻ��ĝ��ڙC(j��)�Ʒ�����
��Ó��(x��)�����|(zh��)�ṩ�����S�h(hu��n)���c���ض��ļ�(x��)���{(di��o)���������P(gu��n)(li��n)����(du��)�ڶ��������ϵ��O(sh��)Ӌ(j��)�����������P(gu��n)��Ҫ�ġ�ԓ�о��M(j��n)һ�������ˌ�(du��)�M����(l��i)ԴÓ��(x��)�����|(zh��)�ĽM�ɳɷ֡��M���خ��Ժ����﹦�ܵ����⣬�U������Ӱ���(j��ng)�ɼ�(x��)�����\(y��n)�����ã�ͬ�r(sh��)Ҳ�(y��n)�C��Ó��(x��)��������|(zh��)ˮ���z�����D(zhu��n)����������ڼ���p���ޏ�(f��)�еľ�����ԓ�������ڰl(f��)����Biomaterials�ϣ�Փ�ĵĵ�һ���ߞ���ɽ��W(xu��)���W(xu��)�W(xu��)Ժ��ʿ�����㟘����ͬͨӍ���ߞ���ɽ��W(xu��)���ϿƌW(xu��)�c���̌W(xu��)Ժȫ��Ƽ���������������c�Ї�(gu��)�ƌW(xu��)Ժ�V�ݽ����c�t(y��)ˎ�о�Ժ����о��T��
��ɽ��W(xu��)ȫ��Ƽ�����n�}�M�F(xi��n)�\(ch��ng)Ƹ��ʿ���c�������ˆT���gӭ���и߷��ӻ��W(xu��)�c�����������t(y��)�ò��ϡ���(x��)��/��������W(xu��)����(d��ng)�(sh��)�(y��n)�Ȍ��I(y��)���������P(gu��n)��(j��ng)�(y��n)�����격ʿ���ˡ����У���Ƹ�о��T����Ƹ���о��T�״�Ƹ�Õr(sh��)���gԭ�t�ϲ����^(gu��)38�ܚq��н�����20~36�f(w��n)Ԫ����š�����(g��)����r���������A(ch��)��λ���Y14~30�f(w��n)+��λ���U(xi��n)һ��+Ч��(j��)��(ji��ng)��0~10�f(w��n)��Ƹ�����꣬��ͬ���ں���m(x��)Ƹ�������]��Ո(q��ng)�����ڼ�����λ���������]����(gu��)��(n��i)��������У��������ʿ���о��T��λ��ԭ�t���������g��35�q���£��@�ò�ʿ�W(xu��)λһ�㲻���^(gu��)���꣬�߂��^�ߵČW(xu��)�g(sh��)ˮƽ���^��(qi��ng)�Ŀ��������ĺ���(n��i)�⃞(y��u)�㲩ʿ����a���W(xu��)У��ʿ�������Y��20�f(w��n)����λ���U(xi��n)һ�𣫿�(j��)Ч��(ji��ng)��0~10�f(w��n)���ṩ���D(zhu��n)ס������Ů��W(xu��)��;��b��������Ӌ(j��)������ʿ����н30�f(w��n)����λ���U(xi��n)һ�𣫿�(j��)Ч��(ji��ng)��0~10�f(w��n)���ṩס������Ů��W(xu��)�ȣ���c���V�|ʡ���齭�˲�Ӌ(j��)������ʿ���Y���(xi��ng)Ŀ��������н30�f(w��n)����λ���U(xi��n)һ�𣫿�(j��)Ч��(ji��ng)��0~10�f(w��n)���ṩס������Ů��W(xu��)�ȣ���վ���^�m(x��)�ڻ������߿ɫ@��40�f(w��n)�����M(f��i)����ʿ���վ������(j��)��(g��)���������]��(j��ng)Ƹ����(j��)�e��λ���̎��͌����Ѝ�λ�������]��(gu��)����C(j��)��(hu��)��(li��n)ϵ��ʽ���]�䣨cesqdp@mail.sysu.edu.cn, �]����(bi��o)�}ע������(y��ng)Ƹ��λ+���I(y��)ԺУ+�������������Ԓ��020-84114030����
Փ��朽ӣ�
https://www.sciencedirect.com/science/article/pii/S0142961220308425
https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.201705739
https://pubs.acs.org/doi/pdf/10.1021/acsami.9b01066
https://www.sciencedirect.com/science/article/pii/S1742706118301910?via%3Dihub
https://www.sciencedirect.com/science/article/pii/S0928493120337103
https://www.liebertpub.com/doi/10.1089/ten.tea.2020.0227
- �Ͼ����I(y��)��W(xu��)ë����/��҂����ڡ��Ͼ���W(xu��)�Ę��t(y��)Ժ�O���ƽ��� AFM��ؓ(f��)�d�ɼ�(x��)������ˮ���z���D(zhu��n)���w�S�� 2026-04-03
- �����ֿƴ��䏩/�ǫI(xi��n)�¡�����������ꐝ�/Ф�i��Nat. Commun.��: �nj�(du��)�Q�H��ˮ���|(zh��)�Y(ji��)��(g��u)�(q��)��(d��ng)����ˮ?d��ng)Uɢ - �s��ˮ���z��(sh��)�F(xi��n)��Ч���ˮ�ռ� 2026-04-02
- ����i Adv. Mater.����x��-�л��i�Y(ji��)��(g��u)��ע�䌧(d��o)�ˮ���z - ��(g��u)����(w��n)���ĽM��-������Ә��� 2026-03-21
- ����������·���ڈF(tu��n)�(du��) AFM���ġ����顱���ֵ��IС������{���w�SĤ - ��(sh��)�F(xi��n)�{��Һ��ͨ�����x 2026-02-25
- ��ɽ��W(xu��)����(qi��ng)�F(tu��n)�(du��) AFM��������Ĥ�˚��{���w�Sˮ���z 2026-01-22
- ����W(xu��)�K�s�����ڈF(tu��n)�(du��) AFM��Һ���{(di��o)���x�ܸ����ܼ{���w�S�����z�O(sh��)Ӌ(j��) 2026-01-14
- �����֙�(qu��n)���ڡ�����ڶ��t(y��)Ժ��С����ڡ�Mater. Today��������3Dܛ֧�ܽY(ji��)��늴̼��{(di��o)����(j��ng)�ɼ�(x��)���ֻ�����(d��o)����p���ޏ�(f��) 2023-12-02
�\(ch��ng)���P(gu��n)ע�߷��ӿƼ�

- ��(gu��)�a(ch��n)���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)��(hu��)�h����...
- ��ˎ����Ч������(j��)����PMEC C...
- 2026����ߌ��Ї�(gu��)��(sh��)�(y��n)�Ұl(f��)չ...
- �����I(l��ng)Ʊح300+���h��I(y��)�R��...
- �P(y��ng)���Ж|�����L���Ѓx�����{(l��n)...
- �f(w��n)����Ŀ �ذ��_(k��i)�֣�2025�C(j��)...
- ICIE��(gu��)�H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_(k��i)չ�ڼ����ۄ�(sh��)������朄�(d��ng)δ...
- 9������Ҋ(ji��n)���£�AI�(q��)��(d��ng)+��(gu��)�a(ch��n)...
- �P(gu��n)���e�k�ڶ�ʮ�����Ї�(gu��)��(gu��)�H...
- �п�Ժ��(d��ng)�������F(tu��n)�(du��) Adv. ...
- �Ͼ����I(y��)��W(xu��)ë����/��҂�...
- �|�ϴ�W(xu��)�����/�����F(tu��n)�(du��) AF...
- �۳Ǵ�Steven Wang���ڡ��^(gu��)...
- �����ֿƴ��䏩/�ǫI(xi��n)�¡���...
- ���������ƾ��_(d��)���ڡ������i...
- �A�ƴ��T�ض����ڈF(tu��n)�(du��) Macro...
- �����������/���t(y��)������� ...
- ������ꐏ�(qi��ng)���ڈF(tu��n)�(du��) Matter...
- �������մ�/���� AFM���w�S...
- �A������߅�������w�i������...